Struktura, lastnosti, nomenklatura in uporaba zlata oksida (III) (Au2O3)
The zlati oksid (III) je anorganska spojina, katere kemijska formula je Au2O3. Teoretično lahko pričakujemo, da je njegova narava kovalentnega tipa. Vendar pa prisotnosti določenega ionskega značaja v njeni trdni snovi ni mogoče v celoti zavreči; ali kaj je isto, predpostavimo odsotnost licence3+ poleg aniona O2-.
Morda se zdi protislovno, da zlato, kot plemenita kovina, lahko rja. V normalnih pogojih kosov zlata (kot so zvezde na spodnji sliki) ni mogoče oksidirati ob stiku s kisikom v atmosferi; vendar pa, kadar je obsevan z ultravijoličnim sevanjem v prisotnosti ozona, OR3, slika je drugačna.

Če bi bile zlate zvezde podvržene tem pogojem, bi postale rdečkastorjave, značilne za Au2O3.
Druge metode za pridobivanje tega oksida bi vključevale kemično obdelavo omenjenih zvezd; na primer pretvarjanje zlate mase v svoj ustrezni klorid, AuCl3.
Potem, na AuCl3, in preostale možne zlitine, ki so nastale, dodamo močan osnovni medij; in s tem dobimo hidrirani oksid ali hidroksid, Au (OH)3. Končno se ta zadnja spojina termično dehidrira, da dobimo Au2O3.
Indeks
- 1 Struktura zlata oksida (III)
- 1.1 Elektronski vidiki
- 1.2 Hidrati
- 2 Lastnosti
- 2.1 Fizični izgled
- 2.2 Molekulska masa
- 2.3 Gostota
- 2.4 Tališče
- 2.5 Stabilnost
- 2.6 Topnost
- 3 Nomenklatura
- 4 Uporabe
- 4.1 Barvanje kozarcev
- 4.2 Sinteza auratov in zagonskega zlata
- 4.3 Ravnanje s samosestavljenimi monosloji
- 5 Reference
Struktura zlata oksida (III)
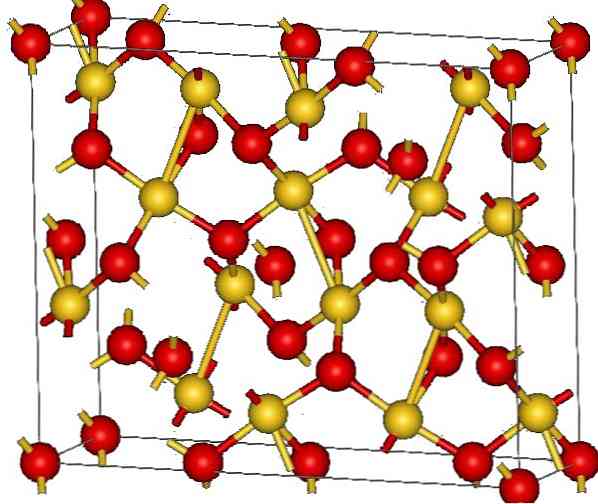
Kristalna struktura zlata (III) oksida je prikazana na zgornji sliki. Prikazana je razporeditev atomov zlata in kisika v trdni snovi, bodisi kot nevtralni atomi (kovalentna trdna snov) ali kot ioni (ionska trdna snov). Nenavadno je dovolj, da v vsakem primeru odpravite ali postavite Au-O povezave.
Glede na sliko se predpostavlja, da prevladuje kovalentni znak (kar bi bilo logično). Zaradi tega so predstavljeni atomi in vezi prikazani s kroglicami oziroma palicami. Zlate krogle ustrezajo zlatim atomom (AuIII-O) in rdečkasto do kisikovih atomov.
Če pozorno pogledate, boste videli, da so na voljo AuO enote4, ki so povezani s kisikovimi atomi. Drug način za vizualizacijo je, da je treba upoštevati, da je vsaka Au3+ je obkrožen s štirimi O2-; Seveda, z ionskega vidika.
Ta struktura je kristalna, ker so atomi urejeni v skladu z enakim dolgoletnim vzorcem. Njegova enotna celica torej ustreza romboedrični kristalni sistem (enako kot na zgornji sliki). Zato vse Au2O3 bi lahko zgradili, če bi bile vse sfere celične celice porazdeljene v prostoru.
Elektronski vidiki
Zlato je prehodna kovina in pričakujemo, da njegove 5d orbitale neposredno vplivajo na 2p orbitale kisikovega atoma. To prekrivanje njihovih orbitalov mora teoretično ustvariti prevodne pasove, ki bi spremenili Au2O3 v trdnem polprevodniku.
Zato je resnična struktura Au2O3 je to še bolj zapleteno.
Hidrati
Zlati oksid lahko zadrži vodne molekule znotraj svojih romboedričnih kristalov, kar povzroča hidrate. Ko nastanejo taki hidrati, postane struktura amorfna, to je neurejena.
Kemijska formula za take hidrate je lahko katera koli od naslednjih snovi, ki dejansko niso globoko pojasnjene: Au2O3. ZH2O (z = 1, 2, 3, itd.), Au (OH)3, ali AuxOin(OH)z.
Formula Au (OH)3 predstavlja pretirano poenostavitev prave sestave omenjenih hidratov. Razlog za to je, da so raziskovalci v zlato hidroksidu (III) ugotovili tudi prisotnost Au2O3; in zato je smiselno, da se ga obravnava izolirano kot "preprost" hidroksid kovinskega prehoda.
Po drugi strani pa trdna s formulo AuxOin(OH)z pričakovati je mogoče amorfno strukturo; od tega je odvisno od koeficientov x, in in z, čigar variacije bi povzročile vse vrste struktur, ki bi lahko komaj pokazale kristalni vzorec.
Lastnosti
Fizični izgled
To je rdečkasto rjava trdna snov.
Molekularna masa
441,93 g / mol.
Gostota
11,34 g / ml.
Tališče
Topi se in razpade pri 160 ° C. Zato nima vrelišča, zato ta oksid nikoli ne doseže vrelišča.
Stabilnost
Au2O3 termodinamično je nestabilen, ker, kot je bilo omenjeno na začetku, zlato v normalnih temperaturnih pogojih ne oksidira. Tako se zlahka zmanjša, da postane ponovno plemenito zlato.
Višja kot je temperatura, hitrejša je reakcija, ki je znana kot termična razgradnja. Torej, Au2O3 pri 160 ° C razpade, da proizvede kovinsko zlato in sprosti molekularni kisik:
2 Au2O3 => 4 Au + 3 O2
Zelo podobna reakcija se lahko pojavi z drugimi spojinami, ki dajejo prednost omenjenemu zmanjšanju. Zakaj zmanjševanje? Ker se zlato vrne, da pridobi elektrone, ki mu je kisik odnesel; kar je isto kot, da izgubi povezave s kisikom.
Topnost
Je trdna snov, netopna v vodi. Vendar pa je topen v klorovodikovi kislini in dušikovi kislini, zaradi nastajanja zlata kloridov in nitratov.
Nomenklatura
Zlati oksid (III) je ime, ki ga ureja nomenklatura zalog. Drugi načini za omembo so:
-Tradicionalna nomenklatura: aurerični oksid, ker je valenca 3+ najvišja za zlato.
-Sistematična nomenklatura: dioro trioksid.
Uporabe
Barvanje kozarcev
Ena izmed njenih najpomembnejših uporab je zagotoviti rdečkaste barve določenim materialom, kot so očala, poleg tega, da dajejo nekatere lastnosti, ki so lastne atomom zlata..
Sinteza auratov in zagonskega zlata
Če se doda Au2O3 na medij, kjer je topen, in v prisotnosti kovin se lahko aurate ob dodatku močne baze oborijo; ki jih tvorijo AuO anioni4- v družbi kovinskih kationov.
Tudi Au2O3 reagira z amoniakom, da tvori zlato polnilno spojino, Au2O3(NH3)4. Njegovo ime izhaja iz dejstva, da je zelo eksplozivno.
Ravnanje s samosestavljenimi enoslojnimi plastmi
Na zlato in njegovem oksidu se nekatere spojine, kot so dialkil disulfidi, RSSR, ne adsorbirajo na enak način. Ko pride do te adsorpcije, se spontano oblikuje Au-S vez, kjer atom žvepla pokaže in definira kemijske lastnosti omenjene površine, odvisno od funkcionalne skupine, na katero je vezana..
RSSR se ne more adsorbirati na Au2O3, na kovinskem zlatu. Zato, če se površina zlata in njegova stopnja oksidacije spremenita, kot tudi velikost delcev ali plasti Au2O3, mogoče je oblikovati bolj heterogeno površino.
Ta površina Au2O3-AuSR sodeluje s kovinskimi oksidi nekaterih elektronskih naprav in tako razvija prihodnje pametnejše površine.
Reference
- Wikipedija. (2018). Gold (III) oksid. Vzpostavljeno iz: en.wikipedia.org
- Kemična formulacija (2018). Zlati oksid (III). Pridobljeno iz: formulacionquimica.com
- D. Michaud. (24. oktober 2016). Zlati oksidi. 911 Metallurgist. Vzpostavljeno iz: 911metallurgist.com
- Shi, R. Asahi in C. Stampfl. (2007). Lastnosti zlatih oksidov Au2O3 in Au2O: Preiskava prvih načel. Ameriško fizično društvo.
- Cook, Kevin M. (2013). Zlati oksid kot maskirna plast za regioselektivno površinsko kemijo. Teze in disertacije. Papir 1460.


