Struktura, lastnosti, sinteza, uporabe in tveganja natrijevega benzoata
The natrijevega benzoata je organska sol, katere kemična formula je C6H5COONa. Proizvaja se ali proizvaja z nevtralizacijsko reakcijo med benzojsko kislino in natrijevim hidroksidom. Rezultat je bela trdna snov (spodnja slika), topna v vodi, in se razgradi s segrevanjem pri 120 ° C.
To sol je naravno prisotna v raznih sadežih in drugih delih zelenjave, kot so: borovnice, slive, rozine, cimet, klinčki in jabolka. Je tudi metabolit alg in rastlin.

Natrijev benzoat se v telesu ne kopiči, saj se hitro združi z aminokislinsko glicinom, da se tvori hipurična kislina, ki se prosto izloča z urinom..
Ta spojina se uporablja s konzervansom za živila, njegovo delovanje pa je bolj učinkovito pri kislem pH. To je posledica prisotnosti organskih kislin, ki živilu dajejo pH, ki je primeren za delovanje natrijevega benzoata; ki kot taki postanejo protonirani v benzojsko kislino.
Ta sol se uporablja tudi pri zdravljenju dednih presnovnih motenj cikla sečnine, ki povzroči kopičenje vmesnega metabolita, za katerega je encim, ki ga obdeluje, pomanjkljiv..
Mednarodni program za kemijsko varnost ni našel škodljivih učinkov natrijevega benzoata na ljudi, za porabo med 647 in 825 mg / kg telesne mase..
Poročali so, da lahko natrijev benzoat povzroči psevdoalergijske reakcije in poslabša simptome pri bolnikih s pogostimi epizodami urtikarije in astme..
Indeks
- 1 Struktura natrijevega benzoata
- 2 Lastnosti
- 2.1 Kemična imena
- 2.2 Fizični opis
- 2.3 Vonj
- 2.4 Okus
- 2.5 Plamenišče
- 2.6 Samodejno vžig
- 2.7 Gostota
- 2.8 Topnost
- 2.9 Stabilnost
- 2.10 Razgradnja
- 2,11 pH
- 2.12 Površinska napetost
- 3 Povzetek
- 4 Uporabe
- 4.1 V hrani
- 4.2 Zdravljenje
- 4.3 Drugo
- 5 Tveganja
- 6 Reference
Struktura natrijevega benzoata
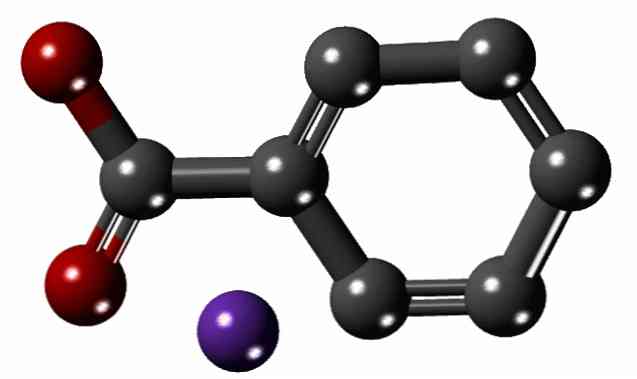
V zgornji sliki je struktura natrijevega benzoata prikazana z modelom kroglic in palic. Aromatski obroč lahko vidimo s prostim očesom s karboksilatno skupino, -COO-, z njo povezane (rdeče sfere); slednji pa elektrostatično privlači Na kation+ (vijolična krogla).
Ker je razlika v velikosti med dvema ionoma velika (primerjajte na sliki), ni presenetljivo, da je reticularna energija kristalov natrijevega benzoata nizka. To povzroča, da imajo njihovi kristali naravno tendenco solubilizirati v polarnih topilih ali da trpijo vrsto kemičnih reakcij.
C6H5COO- Lahko sprejme dva vodikova mostu iz dveh vodnih molekul, kar daje prednost njegovi hidraciji. Medtem, Na+ Konča se tudi solvatirana z vodo, ki premaga elektrostatične sile, ki jo držijo skupaj s C6H5COO-.
Torej je ta sol sestavljena iz C ionov6H5COO- in Na+, ki so urejeni tako, da gradijo kristale. V literaturi ni podatkov o njegovi kristalni strukturi, zato ni znano, kakšna je vrsta celice za to sol.
Lastnosti
Kemična imena
-Natrijev benzoat
-Natrijeva sol benzojske kisline
-Sobenato
-Antimol.
Fizični opis
Bela zrnca ali kristalinični prah. Brezbarvni kristalinični prah.
Vonj
WC.
Okus
Bittersweet, adstrigentno in neprijetno.
Vžigalna točka
> 100 ° C.
Samodejno vžig
> 500 ° C.
Gostota
1,50 g / cm3.
Topnost
-Topen v tekočem amoniju in piridinu.
-Rahlo topen v etanolu: 8,22 g / 100 g pri 25 ° C.
-V metanolu je bolj topen kot v etanolu: 8,22 g / 100 g pri 15 ° C.
Stabilnost
Stabilen je pod priporočenimi pogoji shranjevanja. Lahko je občutljiv na vlago in hidrolizira v benzojsko kislino. Nezdružljivo z močnimi oksidanti, alkalijami in mineralnimi kislinami.
Razgradnja
Ko se segreje do 120 ° C (248 ° F), se oddaja oster dim natrijevega oksida in drugih sestavin, ki so lahko strupene in rakotvorne..
Pri razpadu pri 120 ° C se prepreči natančno določanje vrelišča in tališča, pri čemer so navedene vrednosti teh parametrov teoretične ocene..
pH
Blizu 8, raztopimo v vodi. To je osnovna sol. To je zato, ker hidrolizira, da sprosti OH ione-.
Površinska napetost
72,9 mN / cm pri 20 ° C v raztopini 1 g / l vode.
Sinteza
Benzojska kislina, ki sodeluje pri sintezi natrijevega benzoata, se proizvaja predvsem na tri načine:
-Naftalen se oksidira z vanadijevim pentoksidom, da se tvori ftalni anhidrid. Ta spojina se lahko dekarboksilira, da povzroči benzojsko kislino, saj ima v svoji strukturi z dvema aromatskima obročema dve kondenzirani skupini -COO.
-Toluen se oksidira v benzojsko kislino z dodatkom dušikove kisline. V tej reakciji se metilna skupina "preprosto" oksidira v karboksilno skupino:
C6H5CH3 => C6H5COOH
-In končno, benzotriklorid se hidrolizira z delovanjem mineralnih kislin s poreklom benzojske kisline.
Dobljeno benzojsko kislino po kateri koli od teh treh metod se nato raztopi v natrijevem hidroksidu. Te spojine so podvržene nevtralizacijski reakciji, ki proizvaja natrijev benzoat in vodo.
C6H5COOH + NaOH => C6H5COONa + H2O
Reakcijo lahko izvedemo tudi z natrijevim karbonatom, čeprav je njegov izkoristek lahko manjši od želenega.
Uporabe
V hrani
Natrijev benzoat je sredstvo za konzerviranje hrane, ki lahko zavre ali zadrži proces fermentacije, zakisljevanje ali kateri koli postopek, ki povzroči njihovo poslabšanje. Poleg tega ima natrijev benzoat fungicidno delovanje.
Ta sol je sposobna odstraniti kvasovke, bakterije in glivice, ki so prisotne v hrani. Njegovo konzervativno delovanje je bolj učinkovito pri pH < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Natrijev benzoat se uporablja tudi za konzerviranje gaziranih pijač in brezalkoholnih pijač, v katerih je prisotna karbonska kislina. Tudi v džemih, bogatih s citronsko kislino, in na splošno v živilih s prisotnimi kislinami, ki ustvarjajo kislo okolje.
Poleg tega se uporablja v krmi z koncentracijo natrijevega benzoata 0,1%. Največja uporabljena količina benzojske kisline in natrijevega benzoata kot konzervansov v živilih ne presega 2000 mg / kg hrane..
Zdravljenje
Akutna hiperamonemija
Natrijev fenilacetat in natrijev benzoat se uporabljata v obliki adjuvantnih terapij pri zdravljenju akutne hiperamonemije in povezane encefalopatije pri bolnikih s spremembami ciklusa sečnine..
Te spojine so razvrščene kot zdravila sirote. To poimenovanje velja za zdravila, ki z ekonomskega vidika niso donosna.
Shizofrenija
Natrijev benzoat je bil eksperimentalno uporabljen pri zdravljenju shizofrenije. Osrednji del raziskave je vloga, ki jo ima pri zdravljenju zaviranje encimov oksidaze D-aminokislin, aktivnost, ki ustreza natrijevemu benzoatu..
Arginosukcinska kislina
Natrijev benzoat se uporablja pri zdravljenju argininosukcinske kisline, dedne presnovne motnje, ki lahko pri bolnikih povzroči povečanje koncentracije amonija, ki lahko prizadene centralni živčni sistem..
Inhibitor
-To je zaviralec encima araquidonato 15-lipoksigenaze, encima, ki ga je raziskala farmacevtska industrija zaradi sodelovanja pri koronarni bolezni srca.
-Zavira delovanje lipaznega encima triacilgliceridov, encima, ki deluje na sproščanje glicerola in maščobnih kislin v tankem črevesu, kar omogoča absorpcijo teh lipidov v hrani..
Mogoče je mogoče uporabiti natrijev benzoat za uravnavanje črevesne absorpcije lipidov, kot so triacilgliceridi.
Dedne bolezni
Natrijev benzoat se uporablja pri zdravljenju več dednih bolezni, povezanih s presnovo aminokislin, med katerimi so omenjeni: zdravljenje hiperergininemije in zdravljenje pomanjkanja encimske translokaze ornitina.
Drugi
-Uporablja se pri spiranju na osnovi alkohola in pri poliranju srebra. Poleg tega se uporablja pri izdelavi pirotehničnih spojin, ki so odgovorne za piščalko, ki se proizvaja, ko se vnamejo.
-Uporablja se kot antikorozivna, kar je ena glavnih zahtev pri proizvodnji te soli. Uporablja se tudi v hladilnih, antifriznih in drugih sistemih na vodni osnovi.
-Pri izdelavi plastike, kot je polipropilen, se uporablja za izboljšanje njene trdnosti in jasnosti.
-Služi kot stabilizator v kopalnicah in fotografskih procesih.
Tveganja
Natrijev benzoat je po FDA razvrščen kot "na splošno varen", pri odmerku 0,1% teže živila. Ne šteje, da draži kožo in stik z očmi, zato lahko rečemo, da je akutna toksičnost majhna.
Vendar pa natrijev benzoat lahko povzroči neimunološke reakcije (psevodalergija) v stiku. Ta učinek je pri normalnih ljudeh redka, vendar pri bolnikih s pogostimi epizodami urtikarije ali simptomi astme lahko pride do povečanja pogostosti teh simptomov..
V študijah na podganah in miših niso našli nobenih dokazov o rakotvornem delovanju natrijevega benzoata.
Izpostavili smo neprijetnost njegove uporabe v prisotnosti askorbinske kisline, ki bi lahko proizvajala benzen; toksične spojine, označene kot rakotvorne.
Reference
- Net Industries. (2019). Proizvodnja natrijevega benzoata. Vzpostavljeno iz: science.jrank.org
- Wikipedija. (2019). Natrijev benzoat. Vzpostavljeno iz: en.wikipedia.org
- PubChem. (2019). Natrijev benzoat. Vzpostavljeno iz: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Dejstva o natrijevem benzoatu. Livestrong. Vzpostavljeno iz: livestrong.com
- Kemijska knjiga. (2017). Natrijev benzoat. Vzpostavljeno iz: chemicalbook.com
- Lane H. et al. (2013) Jama Psichiatry. 70 (12): 1267-1275.
- Svetovna zdravstvena organizacija Ženeva. (12. april 2005). Benzojeva kislina in natrijev benzoat. [PDF] Vzpostavljeno iz: who.int


