Izvedba bioloških katalizatorjev in primeri
A biološki katalizator o biokatalizator je molekula, običajno beljakovinskega izvora, ki ima zmožnost pospeševanja kemičnih reakcij, ki se pojavljajo v živih bitjih. Katalitične beljakovinske molekule so encimi, tiste RNA narave pa so ribozimi. V tem članku se bomo osredotočili na raziskovanje encimov, ki so najbolj znani biološki katalizatorji.
V odsotnosti encimov se ogromno število reakcij, ki se odvijajo v celici in omogočajo življenje, ne more pojaviti. Te so odgovorne za pospešitev procesa v velikosti blizu 106 - in v nekaterih primerih veliko večji.
Indeks
- 1 Kataliza
- 2 Encimi
- 2.1 Kaj je encim?
- 2.2 Značilnosti encimov
- 2.3 Nomenklatura in klasifikacija encimov
- 2.4 Kako delujejo encimi?
- 2.5 Encimski inhibitorji
- 2.6 Primeri
- 3 Razlika med biološkimi katalizatorji (encimi) in kemičnimi katalizatorji
- 3.1 Reakcije, ki jih katalizirajo encimi, se pojavijo hitreje
- 3.2 Večina encimov deluje pri fizioloških pogojih
- 3.3 Posebnost
- 3.4 Enzimska ureditev je točna
- 4 Reference
Kataliza
Katalizator je molekula, ki je sposobna spreminjati hitrost kemijske reakcije, ne da bi bila porabljena v omenjeni reakciji.
Kemijske reakcije vključujejo energijo: začetne molekule, ki sodelujejo v reakciji ali reaktanti, se začnejo s stopnjo energije. Dodatna količina energije se absorbira, da se doseže "tranzicijsko stanje". Nato se energija sprosti z izdelki.
Razlika v energiji med reaktanti in produkti je izražena kot ΔG. Če so ravni energije izdelkov večje od reaktantov, je reakcija endergonična in ne spontana. Nasprotno, če je energija izdelkov nižja, je reakcija eksergonična in spontana.
Če pa je reakcija spontana, to ne pomeni, da se bo pojavila z znatno hitrostjo. Hitrost reakcije je odvisna od ΔG * (zvezdica se nanaša na aktivacijsko energijo)..
Bralec mora upoštevati te koncepte, da bi razumel, kako poteka delovanje encimov.
Encimi
Kaj je encim??
Encimi so biološke molekule, ki so izjemno kompleksne in sestoji predvsem iz beljakovin. Proteini so dolge verige aminokislin.
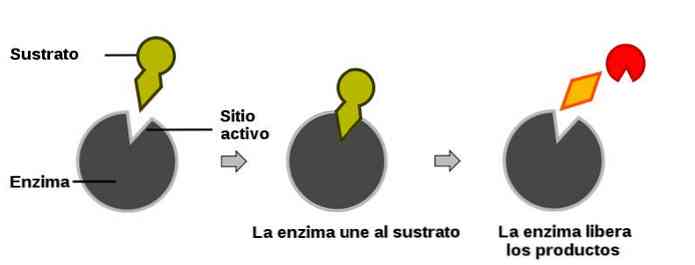
Ena najpomembnejših lastnosti encimov je njihova specifičnost v ciljni molekuli - ta molekula se imenuje substrat..
Značilnosti encimov
Encimi obstajajo v več oblikah. Nekateri so v celoti sestavljeni iz beljakovin, drugi pa imajo ne-proteinske regije, imenovane kofaktorji (kovine, ioni, organske molekule itd.).
Apoenzim je torej encim brez kofaktorja, kombinacija apoenzima in kofaktorja pa se imenuje holoenzim..
So molekule precej velike velikosti. Vendar le majhno mesto encima neposredno sodeluje v reakciji s substratom in ta regija je aktivno mesto.
Ko se reakcija začne, je encim povezan s svojim substratom, ker je ključ povezan s svojo ključavnico (ta model je poenostavitev dejanskega biološkega procesa, vendar služi za ponazoritev procesa).
Vse kemijske reakcije, ki se pojavljajo v našem telesu, katalizirajo encimi. Če teh molekul ni bilo, bi morali čakati na stotine ali tisoče let, da se reakcije dokončajo. Zato je treba regulacijo encimske aktivnosti nadzorovati na zelo specifičen način.
Nomenklatura in klasifikacija encimov
Ko vidimo molekulo, katere ime se konča z -ase, smo lahko prepričani, da je encim (čeprav obstajajo izjeme od tega pravila, kot je tripsin). To je konvencija, ki označuje ime encimov.
Obstaja šest osnovnih vrst encimov: oksidoreduktaze, transferaze, hidrolaze, lijaze, izomeraze in ligaze; odgovoren za: redoks reakcije, prenos atomov, hidrolizo, dodajanje dvojnih vezi, izomerizacijo in vezavo molekul, \ t.
Kako delujejo encimi?
V poglavju o katalizi smo omenili, da je hitrost reakcije odvisna od vrednosti ΔG *. Višja kot je ta vrednost, počasnejša in počasnejša reakcija. Enzim je odgovoren za zmanjšanje navedenega parametra - s tem se poveča hitrost reakcije.
Razlika med produkti in reaktanti ostaja enaka (encim ne vpliva nanj), enako velja tudi za porazdelitev teh produktov. Enzim olajša nastanek prehodnega stanja.
Zaviralci encimov
V okviru študije encimov so inhibitorji snovi, ki uspejo zmanjšati aktivnost katalizatorja. Razvrščamo v dve vrsti: konkurenčne in nekonkurenčne zaviralce. Tisti prve vrste tekmujejo s substratom, drugi pa ne.
Na splošno je proces inhibicije reverzibilen, čeprav lahko nekateri inhibitorji ostanejo vezani na encim skoraj trajno.
Primeri
V naših celicah je veliko encimov - in celic vseh živih bitij. Najbolj znani pa so tisti, ki sodelujejo pri presnovnih poteh, kot so glikoliza, Krebsov cikel, transportna veriga elektronov..
Sukcinat dehidrogenaza je encim tipa oksidoreduktaze, ki katalizira oksidacijo sukcinata. V tem primeru reakcija vključuje izgubo dveh atomov vodika.
Razlika med biološkimi katalizatorji (encimi) in kemičnimi katalizatorji
Obstajajo katalizatorji kemijske narave, ki podobno kot biološki povečujejo hitrost reakcij. Vendar obstajajo opazne razlike med obema vrstama molekul.
Encimsko katalizirane reakcije so hitrejše
Prvič, encimi uspejo povečati hitrost reakcij v velikostnih redih blizu 106 do 1012. Kemijski katalizatorji prav tako povečujejo hitrost, vendar le nekaj vrst.
Večina encimov deluje pri fizioloških pogojih
Ker se biološke reakcije izvajajo znotraj živih bitij, njihovi optimalni pogoji obdajajo fiziološke vrednosti temperature in pH. Kemiki, po drugi strani, potrebujejo drastične pogoje temperature, pritiska in kislosti.
Specifičnost
Encimi so v reakcijah, ki jih katalizirajo, zelo specifični. V večini primerov delajo le z enim substratom ali z nekaj. Posebnost velja tudi za vrsto proizvodov, ki jih proizvajajo. Obseg substratov kemijskih katalizatorjev je veliko širši.
Sile, ki določajo specifičnost interakcije med encimom in njegovim substratom, so enake, ki narekujejo konformacijo istega proteina (Van der Waalsove interakcije, elektrostatične, vodikove vezi in hidrofobne).
Encimska ureditev je natančna
Nazadnje, encimi imajo večjo sposobnost regulacije in njihova aktivnost se spreminja glede na koncentracijo različnih snovi v celici.
Med regulatornimi mehanizmi najdemo alosterično kontrolo, kovalentno modifikacijo encimov in variacijo količine sintetiziranega encima..
Reference
- Berg, J. M., Stryer, L., in Tymoczko, J.L. (2007). Biokemija. Obrnil sem se.
- Campbell, M. K., in Farrell, S. O. (2011). Biokemija Šesta izdaja. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Učbenik biokemije. John Wiley & Sons.
- Koolman, J., in Röhm, K. H. (2005). Biokemija: besedilo in atlas. Ed Panamericana Medical.
- Mougios, V. (2006). Biokemija vadbe. Človeška kinetika.
- Müller-Esterl, W. (2008). Biokemija Osnove medicine in znanosti o življenju. Obrnil sem se.
- Poortmans, J.R. (2004). Načela vadbene biokemije. Karger.
- Voet, D., & Voet, J.G. (2006). Biokemija. Ed Panamericana Medical.


