Kemijska struktura, lastnosti in uporaba amonijevega sulfata
The amonijev sulfat Je ternarna in amoniakalna anorganska sol žveplove kisline. Njegova kemijska formula je (NH4)2SO4. Zato stehiometrični razmerji pravijo, da za vsak sulfatni anion obstajata dve amonijevi kationi, ki sodelujeta z njim. To omogoča nevtralnost soli ((+1) + 2 + (-2)).
Nomenklatura je posledica dejstva, da gre za sol, izpeljano iz H2SO4, spreminjanje pripone "uric" v "ato". Tako sta dva začetna protona nadomeščena z NH4+, reakcijski produkt z amoniakom (NH3). Nato je kemijska enačba za njegovo sintezo: 2 NH3 + H2SO4 => (NH4)2SO4
Amonijev sulfat je skladišče dušika in žvepla, ki sta nepogrešljiva v kemiji tal in gnojil.
Indeks
- 1 Kemijska struktura
- 2 Fizikalne in kemijske lastnosti
- 2.1 Molekularna teža
- 2.2 Fizični izgled
- 2.3 Vonj
- 2.4 Tališče
- 2.5 Topnost
- 2.6 Gostota
- 2.7 Parni tlak
- 2.8 Plamenišče
- 2.9 pH
- 2.10 Stabilnost
- 2.11 Razgradnja
- 2.12 Korozija
- 3 Uporabe
- 3.1 V kmetijstvu
- 3.2 Kot analitski reagent
- 3.3 Pri obarjanju in izolaciji beljakovin
- 3.4 V industriji
- 3.5 Druge uporabe
- 4 Reference
Kemijska struktura
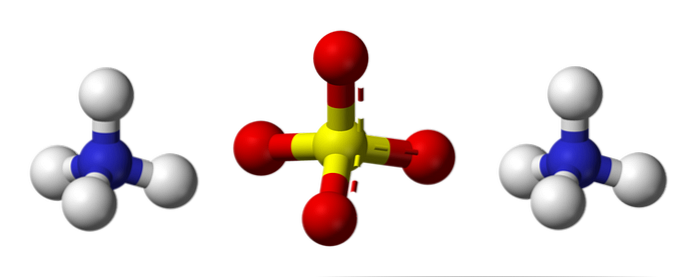
Zgornja slika prikazuje molekularne geometrije ionov NH4+ in SO42-. Rdeče krogle ustrezajo kisikovim atomom, belim kroglicam ustrezajo vodikovi atomi, modre krogle do dušikovega atoma in rumene krogle ustrezajo žveplom.
Oba iona se lahko obravnavata kot dva tetraedra, tako da imata tri enote, ki medsebojno delujejo in tvori ortorombni kristalni dogovor. Sulfatni anion je SO42- in je sposoben podariti ali sprejeti štiri vodikove vezi, tako kot NH kation4+.
Fizikalne in kemijske lastnosti
Molekularna teža
132,134 g / mol.
Fizični izgled
Trdna bela. Ortorombični beli ali rjavi kristali, odvisno od ravni nečistoč.
Vonj
WC.
Tališče
280 ° C. Ta tališče, nizko v primerjavi z drugimi ionskimi spojinami, je posledica dejstva, da je sol z monovalentnimi kationi (+1) in z različnimi ioni v svojih velikostih, zaradi česar ima trdna snov nizko kristalno mrežasto energijo.
Topnost
76,4 g / 100 g vode pri 25 ° C. Ta afiniteta za vodo je posledica velike zmogljivosti njenih molekul za solvat amonijevih ionov. Po drugi strani pa je netopen v acetonu in alkoholu; to je v manj polarnih topilih kot voda.
Gostota
1,77 g / cm3 pri 25 ° C.
Parni tlak
1,871 kPa pri 20 ° C.
Točka vnetljivosti
26 ° C.
pH
5,0-6,0 (25 ° C, 1 M raztopina). Rahlo kisli pH je posledica hidrolize NH4+ v vodi, pri čemer nastane H3O+ pri nizkih koncentracijah.
Stabilnost
Stabilen v primernih okoljskih pogojih. V stiku z močnimi oksidanti se lahko vname.
Razgradnja
Začne se razgraditi pri 150 ° C, pri čemer se sproščajo strupeni hlapi žveplovega oksida, dušikovega oksida in amonija..
Korozija
Ne napada železa ali aluminija.
Uporabe

V kmetijstvu
- Amonijev sulfat se uporablja kot gnojilo v alkalnih tleh. Amonijeva sol ima v svoji sestavi 21% dušika in 24% žvepla. Vendar pa obstajajo spojine, ki zagotavljajo večjo količino dušika kot amonijev sulfat; Prednost slednjega je visoka koncentracija žvepla.
- Žveplo je bistvenega pomena za sintezo beljakovin, saj ima več aminokislin - kot so cistin, metionin in cistein - žveplo. Iz teh razlogov je amonijev sulfat še vedno eno najpomembnejših gnojil.
- Uporablja se v pridelkih pšenice, koruze, riža, bombaža, krompirja, konoplje in sadnega drevja.
- Nizek pH alkalnih tal zaradi njihovega prispevka k procesu nitrifikacije mikrobov. Uporablja se amonij (NH)4+) za proizvodnjo nitrata (NO3-) in sprosti H+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. Povečanje koncentracije vodika zmanjša pH alkalnih tal in omogoča večjo uporabo.
- Amonijev sulfat deluje kot gnojilo kot koadjuvant za topne insekticide, herbicide in fungicide, ki se poškropijo na pridelke..
- Sulfat je sposoben zajeziti ione, prisotne v tleh in v vodi za namakanje, ki so potrebni za življenje določenih patogenov. Med ioni, ki jih ujame amonijev sulfat, so Ca2+, Mg2+, Vera2+ in vero3+. To delovanje poveča mikrobicidni učinek omenjenih sredstev.
Kot analitični reagent
Amonijev sulfat deluje kot sredstvo za obarjanje pri elektrokemični analizi, v mikrobioloških gojiščih in pri pripravi amonijevih soli.
Pri obarjanju in izolaciji beljakovin
Amonijev sulfat se uporablja pri izolaciji in čiščenju proteinov, zlasti plazemskih beljakovin. K določeni koncentraciji plazme dodamo količino amonijevega sulfata; tako nastane obarjanje skupine beljakovin.
Oborino zberemo s centrifugiranjem in supernatantu dodamo dodatno količino amonijevega sulfata in pri novi koncentraciji pride do obarjanja druge skupine proteinov..
Ponovitev prejšnjega postopka v zaporedni obliki omogoča pridobivanje različnih frakcij beljakovin plazme.
Pred uvedbo novih tehnologij molekularne biologije je ta postopek omogočil izolacijo zelo pomembnih beljakovin v medicini, na primer: imunoglobulinov, koagulacijskih faktorjev itd..
V industriji
Amonijev sulfat zavira začetek požara v tekstilni industriji. Uporablja se kot dodatek v industriji galvanizacije. Uporablja se tudi pri proizvodnji vodikovega peroksida, amonijevega klorida itd..
Druge uporabe
- Amonijev sulfat se uporablja kot sredstvo za uravnavanje osmotskega tlaka in kot sredstvo za obarjanje soli.
- V obliki amonijevega lauril sulfata se zmanjša površinska napetost vode, kar omogoča ločevanje onesnaževal s povečanjem trdote vode..
- Je antikorozijsko sredstvo.
- Uporablja se kot aditiv za živila, ki uravnava kislost v testu iz moke in kruhu.
Reference
- OECD SIDS. (Oktober 2004). Amonijev sulfat. [PDF] Vzpostavljeno 27. aprila 2018, iz: inchem.org
- Družba Mosaic. (2018). Amonijev sulfat. Vzpostavljeno 27. aprila 2018, iz: cropnutrition.com
- Wikipedija. (2018). Amonijev sulfat. Vzpostavljeno 27. aprila 2018, z: en.wikipedia.org
- Pubchem. (2018). Amonijev sulfat. Vzpostavljeno 27. aprila 2018, od: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23. julij 2015). [Slika] Vzpostavljeno 27. aprila 2018, s strani flickr.com
- Paula Papp (22. februar 2017). Uporaba in uporaba amonijevega sulfata. Vzpostavljeno 27. aprila 2018, iz: business.com


