Aluminijev sulfat (Al2 (SO4) 3) struktura, uporaba, vrste, toksičnost
The aluminijev sulfat je anorganska aluminijeva sol s formulo Al2(SO4)3, ki se ponavadi pojavi kot bela trdna snov s sijočimi kristali. Na barvo spojine vpliva koncentracija železa in vseh drugih nečistoč. Obstajata dve glavni vrsti aluminijevega sulfata: A in B.
Na spodnji sliki so prikazani beli kristali hidriranega aluminijevega sulfata. Opažamo odsotnost rjavih obarvanosti, ki kažejo na železne ione v kristalni rešetki.

Aluminijev sulfat je sol, ki je zelo topna v vodi in jo v naravi redko najdemo v brezvodni obliki. Ponavadi je hidriran v obliki oktadekahidrata aluminijevega sulfata [Al2(SO4)3.18H2O] ali heksadekahidrat [Al2(SO4)3.16H2O].
Prav tako lahko tvorijo dvojne soli s kalijem in amonijem, spojinami, znanimi kot alumini. Deloma je to lahko posledica afinitete vode v hidratih, da obdrži druge ione poleg aluminija.
Aluminijev sulfat se lahko razgradi z delovanjem vode v aluminijevem hidroksidu in žveplovi kislini. Ta lastnost je omogočila njegovo uporabo kot sredstvo za kisanje tal.
Je tudi strupena spojina, zlasti v stiku s praškom. Vendar pa ima neskončnost uporab in aplikacij, ki segajo od čiščenja vode s pomočjo metode koagulacije, ki se dogaja z njeno uporabo v več panogah, do njene uporabe s terapevtskimi cilji..
Indeks
- 1 Struktura
- 2 Kaj je (uporablja)
- 2.1 Koagulacija ali flokulacija vode
- 2.2 Uporablja se kot jedro črnila in pri izdelavi papirja
- 2.3 Industrijska uporaba
- 2.4 Zdravilne in terapevtske uporabe
- 2.5 Druge uporabe
- 3 Proizvodnja aluminijevega sulfata
- 4 Vrste
- 5 Strupenost
- 6 Reference
Struktura
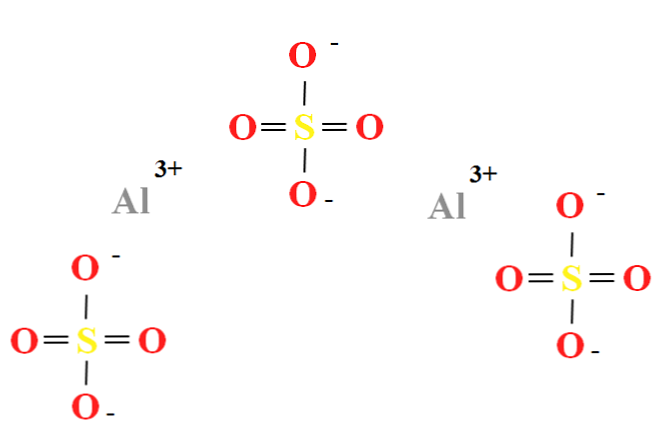
Aluminijev sulfat ima razmerje med dvema kationoma Al3+ za vsake tri anione SO42- (top image), ki jo lahko opazujemo neposredno v njegovi kemijski formuli Al2(SO4)3.
Upoštevajte, da je Al3+ so sive barve, medtem ko SO42- rumene (za atom žvepla) in rdeče (za atome kisika).
Prikazana struktura ustreza brezvodni obliki Al2(SO4)3, ker nobena molekula vode ne vpliva na ione. V vaših hidratih pa lahko vodo privlačijo pozitivni centri Al3+, ali z negativnim SO tetraedrom42- s pomočjo vodikovih vezi (HOH-O-SO32-).
Al2(SO4)318H2Ali, na primer, vsebuje 18 molekul vode v svoji trdni strukturi. Nekateri od njih so lahko v neposrednem stiku z Al3+ ali z obvestilom o nasprotovanju42-. Z drugimi besedami: aluminijev sulfat ima lahko notranjo ali zunanjo koordinacijsko vodo.
Prav tako lahko njegova struktura sprejme druge katione, kot je Fe3+, Na+, K+, itd. Ampak za to je potrebno prisotnost več anionov SO42-. Za kaj? Nevtralizirati povečanje pozitivnih nabojev zaradi kovinskih nečistoč.
Aluminijev sulfat ima lahko veliko struktur, čeprav njegovi hidrati težijo k prevzemu monoklinskega kristalnega sistema.
Fizikalne in kemijske lastnosti
Videz
Pojavi se kot trdna snov z belimi kristali, granulami ali prahom.
Molekularna teža
342,31 g / mol (brezvodni).
Vonj
Brez vonja
Okus
Sladki okus zmerno adstrigenten.
Tališče
Brezvodna oblika 770 ° C (oblika z 86 ° C oktadekahidratada)
Topnost v vodi
31,2 g / 100 ml pri 0 ° C; 36,4 g / 100 ml pri 20 ° C in 89 g / 100 ml pri 100 ° C.
Gostota
2,67 do 2,71 g / cm3.
Topnost
Rahlo topen v etanolu.
Parni tlak
V bistvu nič.
Stabilnost
Stabilen v zraku.
Razgradnja
Ko se segreje na približno tališču, se lahko razgradi z oddajanjem zlasti žveplovega oksida, strupenega plina.
Jedkost
Raztopine aluminijevega sulfata so jedke za aluminij. Prav tako lahko spojina korodira kovine v prisotnosti vlage.
pKa
3,3 do 3,6. Njegov pH je 2,9 ali več v 5% vodni raztopini.
Kaj je za (uporablja)
Koagulacija ali flokulacija vode
-Ko se zmeša z vodo (pitno, postreženo ali odpadno), aluminijev sulfat povzroči aluminijev hidroksid, ki tvori komplekse s spojinami in delce v raztopini, ki pospešuje njihovo sedimentacijo, ki bi v odsotnosti obdelave z aluminijevim sulfatom trajala. dolgo časa.
-Aluminijev sulfat se uporablja tudi pri čiščenju bazenske vode, zaradi česar so bolj privlačni za uporabo.
-Z uporabo aluminijevega sulfata se voda pridobiva brez motnosti in barve, s čimer se poveča njegova zmožnost za čiščenje vode. Žal lahko ta metoda čiščenja privede do rahlo povečane koncentracije aluminija v vodi.
-Aluminij je zelo strupena kovina, ki se nabira v koži, možganih in pljučih in povzroča resne motnje. Poleg tega ni znano, kakšno funkcijo ima v živih bitjih.
-Evropska unija zahteva, da najvišja dovoljena meja aluminija v vodi ne presega 0,2 mg / l. Medtem Agencija ZDA za varstvo okolja zahteva, da najvišja meja onesnaženosti vode z aluminijem ne presega 0,05–0,2 mg / l.
-Obdelava odpadne vode ali uporaba aluminijevega sulfata omogoča ekonomično odstranjevanje ali zmanjševanje fosforja v njih.
Uporabite ga kot jedro črnila in pri izdelavi papirja
-Aluminijev sulfat je bil uporabljen kot sredstvo za barvanje in črnila, kar pomaga pri pritrjevanju materiala, ki ga je treba barvati. Njena določitev je posledica Al (OH).3, katerih želatinasta konsistenca prispeva k adsorpciji barvil na tekstil.
-Čeprav se za opisani namen že od leta 2000 pr. N. Po drugi strani sintetična barvila ne zahtevajo luženja, da bi izpolnila svojo funkcijo.
-Zamenjana je bila s proizvodnjo papirja, vendar se še vedno uporablja pri proizvodnji papirne kaše. Odstranjuje nečistoče in se uporablja za vezanje materialov, nevtralizira naboje in kalibrira kolofonijo.
Industrijska uporaba
-Uporablja se v gradbeni industriji, da bi pospešila postavitev betona. Poleg tega se uporablja pri hidroizolaciji zgradb.
-V industriji mila in maščob se uporablja v proizvodnji glicerina.
-Uporablja se v naftni industriji pri izdelavi sintetičnih katalizatorjev, ki se uporabljajo med obratovanjem.
-V farmacevtski industriji se uporablja kot adstrigentno sredstvo pri pripravi zdravil in kozmetičnih izdelkov.
-Intervenira v proizvodnji barvil, kot je karmin. Uporablja se tudi kot barvilo pri izdelavi sintetičnih kavčukov iz butadien stirena.
-V industriji za proizvodnjo sladkorja se uporablja kot čistilec melase za sladkorni trs.
-Uporablja se pri izdelavi deodorantov. Zakaj? Ker povzroča zoženje vodov znojnih žlez in tako omejuje kopičenje znoja, ki je nujno sredstvo za rast bakterij, ki povzročajo vonj..
-Uporablja se pri strojenju usnja, ki je nujen postopek za njegovo uporabo. Poleg tega se uporablja pri proizvodnji gnojil.
-Uporablja se kot dodatek pri pripravi barv, lepil in tesnilnih mas ter izdelkov za čiščenje in nego pohištva..
Zdravilne in terapevtske uporabe
-Aluminijev sulfat je imunološki adjuvans. Zato izpolnjuje funkcijo obdelave antigenov na tak način, da ko se sprosti na mestu njihovega delovanja, povzroči večjo proizvodnjo protiteles za antigene, ki so bili inokulirani..
-Freundovi adjuvansi in BCG, kot tudi drugi adjuvansi, vključno endogeni, kot so interlevkini, so nespecifični za antigene, kar omogoča povečanje polmera imunskega delovanja. To je omogočilo razvoj cepiv proti številnim boleznim.
-Koagulacijsko delovanje aluminijevega sulfata je omogočilo izločanje številnih virusov v obdelani vodi, med drugim: Q beta, MS2, T4 in P1. Rezultati kažejo, da obdelava vode z aluminijevim sulfatom povzroči inaktivacijo takih virusov.
-Aluminijev sulfat se uporablja v obliki palice ali v obliki praška pri zdravljenju majhnih površinskih ran ali odrgnin, ki nastanejo ob britju..
-Uporablja se pri izdelavi aluminijevega acetata, spojine, ki se uporablja pri zdravljenju nekaterih stanj ušesa. Uporabljen je bil tudi brez znatnega uspeha za lajšanje posledic požarnih mravljinčkov..
-Raztopine aluminijevega sulfata se uporabljajo pri koncentraciji od 5% do 10% pri lokalnem zdravljenju razjed, ki omogočajo nadzor njihovih izločkov..
-Adstrigentno delovanje aluminijevega sulfata kontraktira površinske plasti kože, koagulira beljakovine in zdravi rane.
Druge uporabe
-Aluminijev sulfat pomaga pri nadzoru prekomerne rasti alg v ribnikih, jezerih in vodotokih. Uporablja se tudi pri odstranjevanju mehkužcev, med drugim v španskem polžu.
-Vrtnarji uporabljajo to spojino za kisanje alkalnih tal. V stiku z vodo se aluminijev sulfat razgradi v aluminijev hidroksid in razredčeno žveplovo kislino. Nato se obori aluminijev hidroksid, pri čemer ostane žveplova kislina v raztopini.
-Zakisljevanje tal zaradi žveplove kisline se vizualizira na zelo ustvarjalen način zaradi obstoja rastline, imenovane hortenzije, katere cvetovi postanejo modri v prisotnosti kislih tal; so občutljive in se odzivajo na spremembe pH.
-Aluminijev sulfat sodeluje pri proizvodnji pene za boj proti požaru in nadzor nad njim. Kako? Reagira z natrijevim bikarbonatom, kar povzroči sproščanje CO2. Ta plin blokira dostop O2 na mesto izgorevanja materiala; in posledično premirje, ki se je razvijalo.
Proizvodnja aluminijevega sulfata
Aluminijev sulfat sintetiziramo z reakcijo spojine, bogate z aluminijem, kot je boksitna ruda, z žveplovo kislino pri povišanih temperaturah. Naslednja kemijska enačba predstavlja reakcijo:
Al2O3 + H2SO4 -> Al2(SO4)3 + 3 H2O
Aluminijev sulfat lahko tvorimo tudi z nevtralizacijsko reakcijo med aluminijevim hidroksidom in žveplovo kislino v skladu z naslednjo reakcijo:
2 Al (OH)3 + 3 H2SO4 + 12 H2O -> Al2(SO4)3.18H2O
Žveplova kislina reagira z aluminijem, da nastane amonijev sulfat in sprosti molekule vodika v obliki plina. Reakcija je shematizirana na naslednji način:
2 Al + 3 H2SO4 -> Al2(SO4)3 + 3 H2
Vrste
Aluminijev sulfat je razvrščen v dve vrsti: tip A in tip B. V aluminijevem sulfatu tipa A so trdne snovi bele in imajo koncentracijo železa manj kot 0,5%..
V aluminijevem sulfatu tipa B so trdne snovi rjave in imajo koncentracijo železa manj kot 1,5%.
Obstajajo panoge, ki proizvajajo aluminijev sulfat, ki imajo različne kriterije za razvrstitev. Tako industrija poroča o svoji pripravi aluminijevega sulfata tipa A največjo koncentracijo 0,1% železa kot železovega oksida. Medtem ko za tip B kažejo največjo koncentracijo železa 0,35%.
Strupenost
-Aluminijev sulfat je spojina, ki deluje strupeno v stiku s prahom, kar povzroča draženje kože in v primerih, ko je stik pogost, dermatitis.
-V očeh povzroča močno draženje, tudi pri trajnih poškodbah.
-Vdihavanje povzroča draženje nosu in grla, kar lahko povzroči kašelj in izpuščaje.
-Njegov vnos povzroča draženje želodca, slabost in bruhanje.
-Obstajajo toksični učinki, ki sicer niso neposredno posledica aluminijevega sulfata, ampak so posredno posledica njihove uporabe. Gre za določene toksične učinke aluminija, ki jih povzroča uporaba aluminijevega sulfata pri čiščenju vode.
-Bolniki, ki so kronično dializirani z uporabo soli, pripravljene v prečiščeni vodi, z uporabo aluminijevega sulfata, doživljajo zelo hude zdravstvene motnje. Med temi motnjami imamo anemijo, demenco z dializo in povečanje bolezni kosti.
Reference
- Wikipedija. (2018). Aluminijev sulfat Vzeto iz: en.wikipedia.org
- Aris Industrial Raztopina aluminijevega sulfata tipa A in B. Vzeta iz: aris.com.pe
- Christopher Boyd (9. junij 2014). Top industrijske uporabe za aluminijevega sulfata. Vzeto iz: chemservice.com
- PubChem. (2018). Brezvodni aluminijev sulfat. Vzeto iz: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20. avgust 2009). Varnostni list iz aluminijevega sulfata. [PDF] Vzeto iz: andesia.com
- Kemijska knjiga. (2017). Aluminijev sulfat. Vzeto iz: chemicalbook.com


