Berilijev hidroksid (Be (OH) 2) kemijska struktura, lastnosti in uporaba
The berilijev hidroksid je kemična spojina, sestavljena iz dveh molekul hidroksida (OH) in molekule berilija (Be). Njegova kemijska formula je Be (OH)2 in je značilno, da je amfoterna vrsta. Na splošno lahko dobimo iz reakcije med berilijevim monoksidom in vodo v skladu z naslednjo kemijsko reakcijo: BeO + H2O → Be (OH)2
Po drugi strani pa ima ta amfoterna snov molekularno konfiguracijo linearnega tipa. Vendar se lahko pridobijo različne strukture berilijevega hidroksida: alfa in beta oblika, kot mineralna in v parni fazi, odvisno od uporabljene metode.
Indeks
- 1 Kemijska struktura
- 1.1 Berilijev hidroksid alfa
- 1.2 Beta berilijev hidroksid
- 1.3 Berilijev hidroksid v mineralih
- 1.4 Para berilijevega hidroksida
- 2 Lastnosti
- 2.1 Videz
- 2.2 Termokemične lastnosti
- 2.3 Topnost
- 2.4 Tveganje zaradi izpostavljenosti
- 3 Uporabe
- 4 Pridobitev
- 4.1 Pridobivanje kovinskega berilija
- 5 Reference
Kemijska struktura
To kemično spojino lahko najdete na štiri različne načine:
Berilijev hidroksid alfa
Z dodajanjem katerega koli baznega reagenta, kot je natrijev hidroksid (NaOH) v raztopino berilijeve soli, dobimo alfa (a) obliko berilijevega hidroksida. Primer je prikazan spodaj:
2NaOH (razredčen) + BeCl2 → Be (OH)22 + 2NaCl
2NaOH (razredčen) + BeSO4 → Be (OH)2Na + Na2SO4
Berilijev beta hidroksid
Degeneracija tega alfa produkta tvori meta-stabilno tetragonsko kristalno strukturo, ki se je po daljšem časovnem obdobju spremenila v rombično strukturo, imenovano berilijev hidroksid beta (β)..
To beta obliko dobimo tudi kot oborino iz raztopine natrijevega berilija s hidrolizo v pogojih blizu tališča \ t.
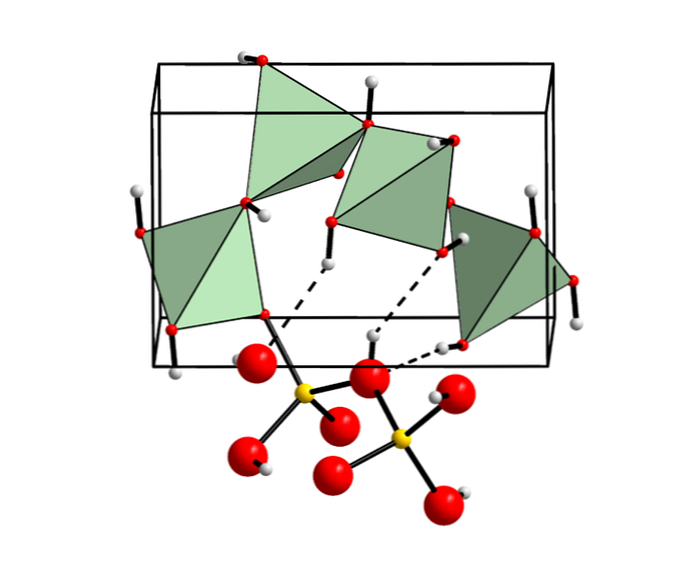
Berilijev hidroksid v mineralih
Čeprav ni običajno, se berilijev hidroksid nahaja kot kristalni mineral znan kot behoite (imenovan na ta način glede na njegovo kemično sestavo)..
Pojavlja se v granitnih pegmatitih, ki nastanejo zaradi spremembe gadolinita (minerali iz skupine silikatov) v vulkanskih fumarolih..
Ta relativno nov mineral je bil prvič odkrit leta 1964, trenutno pa ga najdemo le v granitnih pegmatitih v zveznih državah Teksas in Utah v Združenih državah Amerike..
Para berilijevega hidroksida
Pri temperaturah nad 1200 ° C (2190 ° C) obstaja v parni fazi berilijev hidroksid. Dobljen je iz reakcije med vodno paro in berilijevim oksidom (BeO)..
Podobno ima nastala para parcialni tlak 73 Pa, merjeno pri temperaturi 1500 ° C.
Lastnosti
Berilijev hidroksid ima molsko maso ali približno molekulsko maso 43,0268 g / mol in gostoto 1,92 g / cm.3. Tališče je pri temperaturi 1000 ° C, v kateri se začne razgradnja.
Kot mineral Be (OH)2 (behoita) ima trdoto 4, gostota pa znaša med 1,91 g / cm3 in 1,93 g / cm3.
Videz
Berilijev hidroksid je bela trdna snov, ki ima v obliki alfa želatinast in amorfen izgled. Po drugi strani pa je beta oblika te spojine sestavljena iz dobro opredeljene, ortoromske in stabilne kristalne strukture..
Lahko rečemo, da morfologija mineralov Be (OH)2 je raznolika, saj jo lahko najdemo kot reticularne kristale, drevesne ali sferične agregate. Podobno je bela, roza, modrikasta in celo brezbarvna ter z mastnim steklastim leskom.
Termokemične lastnosti
Entalpija nastanka: -902,5 kJ / mol
Gibbsova energija: -815,0 kJ / mol
Entropija nastajanja: 45,5 J / mol
Toplotna zmogljivost: 62,1 J / mol
Specifična toplotna moč: 1,443 J / K
Standardna entalpija nastanka: -20,98 kJ / g
Topnost
Berilijev hidroksid je po svoji naravi amfoterni, zato je sposoben darovati ali sprejemati protone in raztapljati tako kisle kot bazične medije v kislo-bazni reakciji, pri čemer nastaja sol in voda..
V tem smislu topnost Be (OH)2 v vodi omejuje produkt Kps(H2O), ki je enaka 6,92 × 10-22.
Tveganja izpostavljenosti
Zakonsko dovoljena meja izpostavljenosti ljudi (PEL ali OSHA) snovi berilijevega hidroksida, opredeljena za največjo koncentracijo med 0,002 mg / m3 in 0,005 mg / m3 je 8 ur in pri koncentraciji 0,0225 mg / m3 največ 30 minut.
Te omejitve so posledica dejstva, da je berilij razvrščen kot rakotvorno sredstvo tipa A1 (kancerogeno sredstvo pri ljudeh na podlagi količine dokazov iz epidemioloških študij)..
Uporabe
Uporaba berilijevega hidroksida kot surovine za predelavo nekaterih proizvodov je zelo omejena (in nenavadna). Vendar pa je to spojina, ki se uporablja kot glavni reagent za sintezo drugih spojin in pridobivanje berilijeve kovine.
Pridobivanje
Berilijev oksid (BeO) je kemijska spojina berilija visoke čistosti, ki se najbolj uporablja v industriji. Značilen je kot brezbarvna trdna snov z električno izolacijo in visoko toplotno prevodnostjo.
V tem smislu se postopek za njegovo sintezo (v tehnični kakovosti) v primarni industriji izvaja na naslednji način:
- Berilijev hidroksid se raztopi v žveplovi kislini (H2SO4).
- Ko se reakcija izvede, se raztopina filtrira, tako da se na ta način izločijo netopne nečistoče oksida ali sulfata..
- Filtrat podvržemo uparjenju, da koncentriramo produkt, ki ga ohladimo, da dobimo kristale berilijevega sulfata BeSO.4.
- BeSO4 kalciniramo pri specifični temperaturi med 1100 ° C in 1400 ° C.
Končni proizvod (BeO) se uporablja za proizvodnjo posebnih keramičnih kosov za industrijsko uporabo.
Pridobivanje kovinskega berilija
Med ekstrakcijo in predelavo berilijevih mineralov nastajajo nečistoče, kot so berilijev oksid in berilijev hidroksid. Slednji je podvržen vrsti transformacij do pridobitve kovinskega berilija.
Be (OH) reagira2 z raztopino amonijevega bifluorida: \ t
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BeF4 + 2H2O
(NH4)2BeF4 je podvržen povišanju temperature, ki ima toplotno razgradnjo:
(NH4)2BeF4 → 2NH3 + 2HF + BeF2
Končno zmanjšanje berilijevega fluorida pri temperaturi 1300 ° C z magnezijem (Mg) povzroči nastanek berilijeve kovine: \ t
BeF2 + Mg → Be + MgF2
Berilij se uporablja v kovinskih zlitinah, proizvodnji elektronskih komponent, proizvodnji sevalnih zaslonov in oken, ki se uporabljajo v rentgenskih aparatih.
Reference
- Wikipedija. (s.f.). Berilijev hidroksid. Vzpostavljeno iz en.wikipedia.org
- Holleman, A.F. Wiberg, E. in Wiberg, N. (2001). Berilijev hidroksid. Vzpostavljeno iz books.google.co.ve
- Publishing, M.D. (s.f.). Behoite. Vzpostavljeno iz handbookofmineralogy.org
- Vse reakcije. (s.f.). Berilijev hidroksid Be (OH)2. Vzpostavljeno iz allreactions.com
- PubChem. (s.f.). Berilijev hidroksid. Vzpostavljeno iz pubchem.ncbi.nlm.nih.gov
- Walsh, K.A. in Vidal, E.E. (2009). Kemija in predelava berilija. Vzpostavljeno iz books.google.co.ve


