Kemična struktura, lastnosti, uporaba aluminijevega klorida (AlCl3)
The aluminijev klorid ali aluminijev triklorid (AlCl3) je binarna sol, ki jo tvori aluminij in klor. Včasih je videti kot rumeni prašek, ker predstavlja nečistoče zaradi prisotnosti železovega (III) klorida.
Dobimo jo z združevanjem njenih elementov. Aluminij, ki ima na svojem zadnjem energetskem nivoju tri elektrone (družina IIIA), se nagiba k temu, da jih pridobi zaradi svoje kovinske narave. Klor s sedmimi elektroni v svoji zadnji energijski ravni (družina VIIA) jih nagiba k pridobivanju okteta.
Šteje se, da je vez med aluminijem in klorom v aluminijevem trikloridu kovalentna, čeprav gre za povezavo med kovino in nekovinskim materialom..
Obstajata dve vrsti aluminijevega klorida:
- Brezvodni aluminijev klorid. AlCl3.
- Aluminijev klorid heksahidrat. AlCl3. 6H2To spojino lahko najdemo v trdni obliki ali obliki raztopine.
Indeks
- 1 Kemijska struktura
- 2 Lastnosti
- 2.1 Fizično
- 2.2 Kemikalija
- 3 Uporabe
- 4 Tveganja: možni učinki
- 5 Priporočila
- 6 Reference
Kemijska struktura
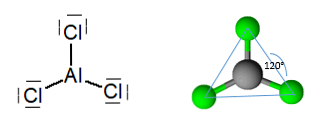
Brezvodni aluminijev triklorid je molekula z ravninsko trigonsko geometrijo s kotom 120 °, ki ustreza atomski hibridizaciji.2.
Vendar je molekula organizirana v obliki dimeri, pri čemer atom klora podari par elektronov za tvorbo vezi. Te so znane kot koordinirane kovalentne vezi.
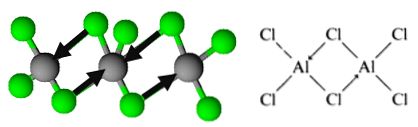
Tako se ugotovi organizacija dimerij aluminijevega triklorida.
Ta organizacija omogoča spojini, da oblikuje mreže dimernih plasti. Kadar se na trdni aluminijev triklorid vlije voda, se ne razgrajujejo, kot se pričakuje, od ionskih spojin, temveč se močno hidrolizira..
Nasprotno, v razredčeni vodni raztopini so koordinirani ioni [Al (H2O)6]+3 in klorid. Te strukture so zelo podobne strukturam diborana.
Na ta način imate formulo Al2Cl6
Če se izmeri razlika v elektronegativnosti atomov, ki sestavljajo vezi v tej spojini, je mogoče opaziti naslednje:
Za aluminij Al je vrednost elektronegativnosti 1,61 C, klor pa 3,16 C. Razlika v elektronegativnosti je 1,55 ° C..
V skladu s pravili zavezujoče teorije, da je spojina ionska, mora imeti razliko v elektronegativnosti atomov, ki tvorijo vez vrednosti večjo ali enako 1,7 C.
V primeru povezave Al-Cl je razlika v elektronegativnosti 1,55 ° C, kar daje aluminijev triklorid kovalentno vezalno ureditev. To majhno vrednost lahko pripišemo koordiniranim kovalentnim vezem, ki jih predstavlja molekula.
Lastnosti
Fizično
Videz: bela trdna, včasih rumena zaradi nečistoč, ki jih povzroča železov klorid
Gostota: 2,48 g / ml
Molarna masa%: 133,34 g / mol
Sublimacija: sublimira pri 178 ° C, zato so tališča in vrelišča zelo nizka.
Vožnja: slabo vodi elektriko.
Topnost: ni topen v vodi, ker je Lewisova kislina. Topen je v organskih topilih, kot so benzen, ogljikov tetraklorid in kloroform.
Kemikalije
V vodi se aluminijev triklorid hidrolizira, pri čemer se tvori HCl in hidronijev ion in aluminijev hidroksid:
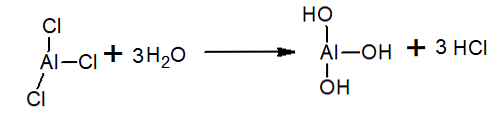
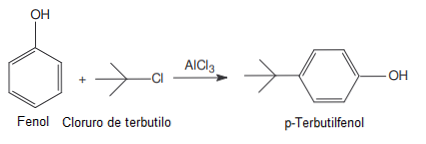
Uporablja se v Friedel-Craftsovih reakcijah kot katalizator (snov, ki jo je mogoče ob koncu reakcije izločiti, ker je le v njej pospešiti, upočasniti ali sprožiti reakcijo).
Je jedka snov.
Pri razpadu, ko burno reagira z vodo, nastane aluminijev oksid in nevarni plini, kot je klorovodik.
Uporabe
- Antiperspirant.
- Katalizator v acilaciji in alkilaciji Friedel-Crafts.
Tveganja: možni učinki
- Je jedka snov, povzroča opekline na koži in resne poškodbe oči.
- Burno reagira z vodo.
- To je nevarno za okolje.
- Zelo strupeno za vodne organizme.
Priporočila
Izogibajte se izpostavljanju izdelku brez potrebnih varnostnih ukrepov. Uporabiti je treba zaščitna očala, rokavice, ustrezna oblačila, pokrit čevelj.
V primeru vdihavanja. Vdihavanje prahu lahko povzroči draženje dihalnih poti zaradi jedke lastnosti snovi. Simptomi vključujejo vneto grlo, kašelj in zasoplost. Simptomi pljučnega edema so lahko pozni in težki so lahko usodni. Žrtev premaknite na zračen prostor brez onesnaževalcev. po potrebi zagotovite umetno dihanje. Če imate težave z dihanjem, zagotovite kisik. Pokličite zdravnika.
V primeru stika s kožo. AlCl3 Je jedka. Lahko povzroči draženje ali opekline z rdečico in bolečino. Takoj po končanem stiku z vodo najmanj 20 minut. Ne nevtralizirajte ali dodajte snovi, ki niso voda. Odstranite kontaminirana oblačila in jih pred ponovno uporabo operite. v primeru poškodbe se takoj posvetujte z zdravnikom.
Ob stiku z očmi. AlCl3 Je jedka. Povzroča močno bolečino, zamegljen vid in poškodbe tkiva. Takoj očistite oči z vodo vsaj 20 minut in odprite veke, da se očisti celotno oko in tkiva veke. Izpiranje oči v nekaj sekundah je bistveno za doseganje maksimalne učinkovitosti. Če imate kontaktne leče, jih odstranite po prvih 5 minutah in nato nadaljujte z izpiranjem oči. Posvetujte se z zdravnikom. Lahko povzroči resno poškodbo roženice, veznice ali drugih delov očesa.
V primeru zaužitja. AlCl3 Je jedka. Opekline lahko povzročijo bolečine v ustih in požiralniku ter opekline sluznice. Lahko povzroči neugodje v prebavilih zaradi bolečin v trebuhu, slabosti, bruhanja in driske. NE POUDARJAJTE. Sperite usta in popijte vodo. Nikoli ne dajte ničesar ustno nezavestni osebi. Pokličite zdravnika. Če pride do spontanega bruhanja, postavite žrtev na njegovo ali njeno stran, da zmanjšate tveganje aspiracije.
Osebe z obstoječimi kožnimi boleznimi ali težavami z očmi ali okvarjeno dihalno funkcijo so lahko bolj dovzetne za učinke snovi
Pakiranje in shranjevanje AlCl spojine3 opraviti v zračenih, čistih in suhih prostorih.
Reference
- Chemical book, (2017), Aluminijev klorid. Izterjano iz chemicalbook.com
- kozmos na spletu, cosmos.com.mx
- Sharpe, A.G., (1993), Organska kemija, Španija, Editorial Reverté, S.A..
- F., (2017), AlCl aluminijev klorid3, Insignia. Vzeto izblog.elinsignia.com.
- TriHealth, (2018), aluminijev triklorid, zadnja posodobitev, 4. marec 2018, Vzpostavljeno iz trihealth.adam.com.
- RxWiki, (s.f), aluminijev klorid, pridobljeno iz, rxwiki.com.


