Uravnoteženje kemijskih enačb Metode in primeri
The uravnoteženje kemijskih enačb pomeni, da imajo vsi elementi v enačbi enako število atomov na vsaki strani. Da bi to dosegli, je treba uporabiti metode uravnoteženja, da se dodelijo stehiometrični koeficienti, primerni za vsako vrsto, prisotno v reakciji..
Kemična enačba je predstavitev s pomočjo simbolov, kaj se dogaja med kemično reakcijo med dvema ali več snovmi. Reaktanti medsebojno delujejo in odvisno od reakcijskih pogojev dobimo eno ali več različnih spojin kot produkt..
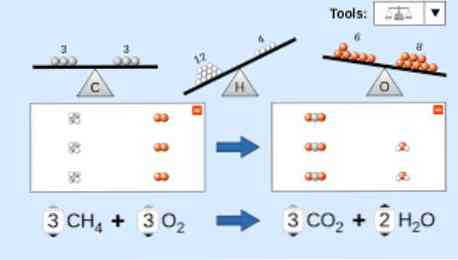
Pri opisovanju kemijske enačbe je treba upoštevati naslednje: Najprej se reaktantske snovi zapišejo na levi strani enačbe, sledi pa ena puščica ali dve nasprotni vodoravni puščici, odvisno od vrste reakcije, ki se izvaja. rt.
Indeks
- 1 Metode uravnoteženja kemijskih enačb
- 1.1 Bilanca kemijskih enačb s poskusi in napakami (imenovana tudi s pregledom ali poskusom)
- 1.2 Algebraično uravnoteženje kemijskih enačb
- 1.3 Valjanje redoks enačb (ion-electron metoda)
- 2 Primeri uravnoteženja kemijskih enačb
- 2.1 Prvi primer
- 2.2 Drugi primer
- 2.3 Tretji primer
- 3 Reference
Metode uravnoteženja kemijskih enačb
Če upoštevamo, da so reaktanti in produkti znani in da so njihove formule pravilno izražene na strani, ki jim ustreza, nadaljujemo z uravnoteženjem enačb po naslednjih metodah:.
Uravnoteženje kemijskih enačb s poskusi in napakami (imenovano tudi s pregledom ali poskusom)
Temelji na stehiometriji reakcije in poskuša poskusiti z različnimi koeficienti, da bi uravnotežili enačbo, dokler izberemo najmanjše možne cele številke, s katerimi dobimo enako število atomov vsakega elementa na obeh straneh. reakcije.
Koeficient reaktanta ali izdelka je število, ki je pred njegovo formulo, in je edino število, ki se lahko spremeni pri uravnoteženju enačbe, saj bi spreminjanje indeksov formul spremenilo identiteto spojine. vprašanje.
Preštejte in primerjajte
Ko smo identificirali vsak element reakcije in ga postavili na pravo stran, nadaljujemo s štetjem in primerjavo števila atomov vsakega elementa v enačbi in določimo tiste, ki morajo biti uravnotežene..
Nato nadaljujemo z uravnoteženjem vsakega elementa (enega naenkrat), tako da pred vsako formulo postavimo cele koeficiente, ki vsebujejo neuravnotežene elemente. Običajno so kovinski elementi najprej uravnoteženi, nato pa nekovinski elementi in končno kisikov in vodikov atom.
Na ta način vsak koeficient pomnoži vse atome predhodne formule; tako da lahko pri uravnoteženju elementa drugi neuravnoteženi, vendar se to popravi, ko je reakcija uravnotežena.
Nazadnje, potrjuje ga zadnje štetje, da je celotna enačba pravilno uravnotežena, to je, da se drži zakona ohranjanja snovi.
Algebraično uravnoteženje kemijskih enačb
Za uporabo te metode se vzpostavi postopek za obravnavo koeficientov kemijskih enačb kot neznanih sistemov, ki jih je treba rešiti..
Najprej se za referenco vzame določen element reakcije, koeficienti pa se postavijo kot črke (a, b, c, d ...), ki predstavljajo neznanke glede na obstoječe atome tega elementa v vsaki molekuli (če vrsta ne vsebuje elementa, ki je uvrščen "0").
Po pridobitvi te prve enačbe določimo enačbe za druge elemente, ki so prisotni v reakciji; obstajalo bo toliko enačb, kolikor je elementov v omenjeni reakciji.
Nazadnje, neznanke določimo z eno od algebraičnih metod redukcije, izenačevanja ali zamenjave in koeficiente dobimo, da dobimo pravilno uravnoteženo enačbo..
Uravnoteženje redoks enačb (ion-electron metoda)
Najprej se splošna (neuravnotežena) reakcija postavi v njeno ionsko obliko. Nato se ta enačba razdeli na dve pol-reakciji, oksidacijo in redukcijo, pri čemer je vsaka uravnoteženost glede na število atomov, njihov tip in naboje teh..
Na primer, za reakcije, ki se pojavljajo v kislem mediju, se dodajo H molekule.2Ali za uravnoteženje kisikovih atomov in dodajanje H+ za uravnoteženje vodikovih atomov.
Nasprotno pa je v alkalnem mediju dodano enako število OH ionov- na obeh straneh enačbe za vsak H ion+, in kjer nastajajo ioni H+ in OH- združujejo se v molekule H2O.
Dodaj elektrone
Nato morate dodati toliko elektronov, kot je potrebno za uravnoteženje nabojev, po uravnoteženju snovi v vsaki polovični reakciji.
Po zvijanju vsake pol-reakcije se te dodajo in dosežejo vrhunec z uravnoteženjem končne enačbe s poskusi in napakami. V primeru razlike v številu elektronov obeh pol-reakcij, je treba eno ali oba pomnožiti s koeficientom, ki je enak tej številki.
Nazadnje je treba potrditi, da enačba vključuje enako število atomov in isto vrsto atomov, poleg tega, da imajo enake naboje na obeh straneh globalne enačbe..
Primeri uravnoteženja kemijskih enačb
Prvi primer
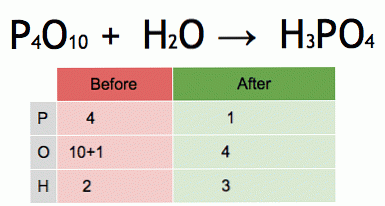
To je animacija uravnotežene kemijske enačbe. Fosforjev pentoksid in voda se pretvorita v fosforno kislino.
P4O10 + 6 H2O → 4 H3PO4 (-177 kJ).
Drugi primer
Imate reakcijo zgorevanja etana (neuravnoteženo).
C2H6 + O2 → CO2 + H2O
Z metodo poskusov in napak, da bi jo uravnotežili, opazimo, da nobeden od elementov nima enakega števila atomov na obeh straneh enačbe. Tako se začne z ravnotežjem ogljika in doda dve kot stehiometrični koeficient, ki ga spremlja na strani izdelkov.
C2H6 + O2 → 2CO2 + H2O
Ogljik je uravnotežen na obeh straneh, zato nadaljujemo z uravnoteženjem vodika tako, da dodamo tri molekule vode.
C2H6 + O2 → 2CO2 + 3H2O
Končno, ker na desni strani enačbe obstaja sedem kisikovih atomov in je zadnji element, ki je še vedno uravnotežen, je pred molekulo kisika postavljeno delno število 7/2 (čeprav so na splošno prednostni celotni koeficienti).
C2H6 + 7 / 2O2 → 2CO2 + 3H2O
Potem preverite, da je na vsaki strani enačbe enako število atomov ogljika (2), vodika (6) in kisika (7)..
Tretji primer
Oksidacija železa v dikromatnih ionih poteka v kislem mediju (neuravnotežena in v svoji ionski obliki)..
Vera2+ + Cr2O72- → Vera3+ + Cr3+
S pomočjo ion-elektronske metode za uravnoteženje je razdeljena na dve pol-reakciji.
Oksidacija: Vera2+ → Vera3+
Redukcija: Cr2O72- → Cr3+
Ker so atomi železa že uravnovešeni (1: 1), se na stran produktov doda elektron, ki uravnava naboj.
Vera2+ → Vera3+ + e-
Zdaj so atomi Cr uravnovešeni in dodajo dve na desno stran enačbe. Nato, ko se reakcija odvija v kislem mediju, dodamo sedem H molekul.2Ali na strani proizvodov za uravnoteženje kisikovih atomov.
Cr2O72- → 2Cr3+ + 7H2O
Za uravnoteženje atomov H dodamo štirinajst H ionov+ na strani reaktantov in po izenačevanju materiala se naboji uravnavajo z dodatkom šestih elektronov na isti strani.
Cr2O72- +14H+ + 6e- → 2Cr3+ + 7H2O
Na koncu dodamo obe pol-reakciji, vendar ker je v oksidacijski reakciji samo en elektron, je treba vse to pomnožiti s šestimi..
6Fe2+ + Cr2O72- +14H+ + 6e- → Vera3+ + 2Cr3+ + 7H2O + 6e-
Končno, elektrone je treba odstraniti na obeh straneh globalne ionske enačbe, preveriti, da sta njihova polnitev in snov pravilno uravnoteženi.
Reference
- Chang, R. (2007). Kemija (9. izd.). McGraw-Hill.
- Hein, M., in Arena, S. (2010). Temelji College Chemistry, Alternate. Vzpostavljeno iz books.google.co.ve
- Tuli, G. D., in Soni, P. L. (2016). Jezik kemije ali kemijske enačbe. Vzpostavljeno iz books.google.co.ve
- Speedy Publishing (2015). Kemijske enačbe in odgovori (Speedy Study Guides). Vzpostavljeno iz books.google.co.ve


