Lastnosti kalijevega jodata, struktura, uporaba in tveganja
The kalijevega jodata ali kalijev jodat je anorganska spojina joda, zlasti sol, katere kemijska formula je KIO3. Jod, element skupine halogenov (F, Cl, Br, I, As), ima v tej soli oksidacijsko število +5; zaradi tega je močno oksidacijsko sredstvo. KIO3 disociira v vodnem mediju, da nastane K ione+ in IO3-.
Sintetizira se z reagiranjem kalijevega hidroksida z jodno kislino: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Prav tako ga lahko sintetiziramo z reagiranjem molekulskega joda s kalijevim hidroksidom: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

Indeks
- 1 Fizikalne in kemijske lastnosti
- 1.1 Oksidacijsko sredstvo
- 2 Kemijska struktura
- 3 Uporaba in uporaba kalijevega jodata
- 3.1 Terapevtska uporaba
- 3.2 Uporaba v industriji
- 3.3 Analitska uporaba
- 3.4 Uporaba v tehnologiji laserjev
- 4 Tveganja za zdravje s kalijevim jodatom
- 5 Reference
Fizikalne in kemijske lastnosti
Bela trdna snov brez vonja, z drobnimi kristali in kristalno strukturo monoklinskega tipa. Ima gostoto 3,98 g / ml, molekulsko maso 214 g / mol in absorpcijske pasove v infrardečem (IR) spektru..
Ima tališče: 833 ºK (560 ºC), skladno z močnimi ionskimi interakcijami med K ioni+ in IO3-. Pri višjih temperaturah pride do reakcije termične razgradnje, ki sprosti molekulski kisik in kalijev jodid:
2KIO3(s) => 2KI (s) + 3O2(g)
V vodi ima topnost, ki se giblje od 4,74 g / 100 ml do 0 ° C, do 32,3 g / 100 ml pri 100 ° C, kar ustvarja brezbarvne vodne raztopine. Poleg tega je netopen v alkoholu in dušikovi kislini, vendar je topen v razredčeni žveplovi kislini.
Njena afiniteta za vodo ni opazna, kar pojasnjuje, zakaj ni higroskopična in ne obstaja v obliki hidriranih soli (KIO).3· H2O).
Oksidacijsko sredstvo
Kalijev jodat, kot je razvidno iz njegove kemijske formule, ima tri kisikove atome. To je močno elektronegativni element in zaradi te lastnosti "razkriva" elektronsko pomanjkljivost v oblaku, ki obdaja jod..
Ta pomanjkljivost ali prispevek se lahko izračuna kot oksidacijsko število joda (± 1, +2, +3, +5, +7), pri čemer je +5 pri tej soli..
Kaj to pomeni? Da jih bo joda, preden bo sposobna pridobiti svoje elektrone, sprejeti v svoji ionski obliki (IO)3-) postane molekularni jod in ima oksidacijsko število 0.
Po tej razlagi je mogoče ugotoviti, da je kalijev jodat oksidativna spojina, ki močno reagira z reducenti pri mnogih redoks reakcijah; od vseh teh je ena znana kot jodna ura.
Jodna ura je sestavljena iz redoks procesa počasnih in hitrih korakov, pri čemer hitre korake označuje rešitev KIO3 v žveplovi kislini, ki ji je dodan škrob. Nato škrob - nekoč proizveden in zasidran med njegovo strukturo vrste I3-- bo spremenila raztopino iz brezbarvne v temno modro.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6 H+ → 3 I2 + 3 H2O
I2 + HSO3- + H2O → 2 I- + HSO4- + 2H+ (temno modra zaradi učinka škroba)
Kemijska struktura
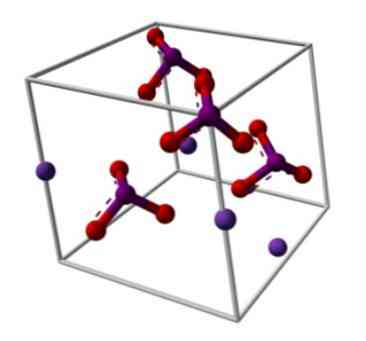
Kemična struktura kalijevega jodata je prikazana na zgornji sliki. IO anion3- predstavlja "trinožnik" rdečih in vijoličnih kroglic, medtem ko so K ioni+ predstavljajo jih vijolične krogle.
Kaj pa pomenijo ti stativi? Pravilne geometrijske oblike teh anionov so dejansko trigonalne piramide, v katerih kisiki tvorijo trikotno osnovo, ne-deljeni par elektronov v jodu pa kaže navzgor, zaseda prostor in silijo IO povezavo navzdol in dva povezave I = O.
Ta molekularna geometrija ustreza sp hibridizaciji3 osrednjega jodovega atoma; druga perspektiva pa nakazuje, da eden od kisikovih atomov tvori vezi z "d" orbitali joda, ker je dejansko sp hibridizacija3d2 (jod ima lahko "d" orbitale, ki širijo valentno lupino).
Kristali te soli so lahko podvrženi prehodom strukturne faze (drugačna ureditev kot monoklinska) kot posledica različnih fizikalnih pogojev, ki jih izpostavljajo.
Uporaba in uporaba kalijevega jodata
Terapevtska uporaba
Kalijev jodat se običajno uporablja za preprečevanje kopičenja radioaktivnosti v ščitnici v obliki 131I, kadar se ta izotop uporablja pri določanju vnosa joda s ščitnico kot sestavine delovanja ščitnice.
Podobno se kalijev jodat uporablja kot topikalni antiseptik (0,5%) pri okužbah sluznice..
Uporaba v industriji
Doda se krmi domačih živali kot dodatek joda. Zato se v industriji kalijev jodat uporablja za izboljšanje kakovosti moke.
Analitska uporaba
V analitski kemiji se zaradi svoje stabilnosti uporablja kot primarni standard pri standardizaciji standardnih raztopin natrijevega tiosulfata (Na2S2O3), da bi določili koncentracije joda v vzorcih.
To pomeni, da so količine joda znane po volumetričnih tehnikah (titracija). V tej reakciji kalijev jodat hitro oksidira jodidne ione I-, z naslednjo kemijsko enačbo:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jod, jaz2, naslovimo z raztopino Na2S2O3 za njegovo standardizacijo.
Uporaba v tehnologiji laserjev
Študije so pokazale in potrdile zanimive piezoelektrične, piroelektrične, elektrooptične, feroelektrične lastnosti in nelinearno optiko kristalov KIO.3. To ima za posledico velik potencial v elektronskem polju in tehnologiji laserjev za materiale, izdelane s to spojino.
Zdravstveno tveganje kalijevega jodata
V visokih odmerkih lahko povzroči draženje ustne sluznice, kože, oči in dihalnega trakta.
V preskusih toksičnosti kalijevega jodata pri živalih je bilo mogoče opaziti, da pri psih, ki so postili, pri odmerkih 0,2–0,25 g / kg telesne teže, ki se daje oralno, povzroča bruhanje.
Če se ti bruhanjem izognemo, povzroči poslabšanje stanja pri živalih, saj povzroči anoreksijo in umiranje pred smrtjo. Njegova obdukcija je omogočila opazovanje nekrotičnih lezij v jetrih, ledvicah in črevesni sluznici.
Zaradi svoje oksidacijske moči predstavlja nevarnost požara, ko pride v stik z vnetljivimi materiali.
Reference
- Day, R., & Underwood, A. Kvantitativna analitična kemija (peta izdaja). PEARSON Prenticeova dvorana, str.
- Muth, D. (2008). Laserji. Vzpostavljeno iz: flickr.com
- Chemical Book. (2017). Kalijev jodat. Pridobljeno 25. marca 2018 iz ChemicalBook: chemicalbook.com
- PubChem. (2018). Kalijev jodat. Pridobljeno 25. marca 2018, iz PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Kalijev jodat. Pridobljeno 25. marca 2018 iz podjetja Merck:
- merckmillipore.com
- Wikipedija. (2017). Kalijev jodat. Pridobljeno 25. marca 2018 iz Wikipedije: en.wikipedia.org
- M M Abdel Kader et al. (2013). Mehanizem prenosa polnjenja in nizki temperaturni fazni prehodi v KIO3. J. Phys.: Conf. Ser 423 012036


