Struktura, lastnosti in uporaba kalcijevega oksida (CaO)
The kalcijev oksid (CaO) je anorganska spojina, ki vsebuje kalcij in kisik v ionskih oblikah (ne smemo zamenjevati s kalcijevim peroksidom, CaO).2). Znana je po vsem svetu kot apno, beseda, ki označuje katero koli anorgansko spojino, ki vsebuje karbonate, kalcijeve okside in hidrokside, kot tudi druge kovine, kot so silicij, aluminij in železo..
Ta oksid (ali apno) se prav tako kolokvijalno omenja kot apno ali gašeno apno, odvisno od tega, ali je hidriran ali ne. Apno je kalcijev oksid, medtem ko je gašeno apno njegov hidroksid. Po drugi strani je apnenec (apnenec ali utrjen apnen) dejansko sedimentna kamnina, sestavljena predvsem iz kalcijevega karbonata (CaCO).3).

Je eden največjih naravnih virov kalcija in je surovina za proizvodnjo kalcijevega oksida. Kako nastane ta oksid? Karbonati so dovzetni za toplotno razgradnjo; ogrevanje kalcijevih karbonatov pri temperaturah nad 825 ° C, kar vodi do nastanka apna in ogljikovega dioksida.
Zgoraj navedeno izjavo lahko opišemo na naslednji način: CaCO3(s) → CaO (s) + CO2(g) Ker je zemeljska skorja bogata z apnencem in kalcitom, v oceanih in plažah pa so obilne morske školjke (surovine za proizvodnjo kalcijevega oksida), kalcijev oksid relativno poceni reagent.
Indeks
- 1 Formula
- 2 Struktura
- 3 Lastnosti
- 3.1 Topnost
- 4 Uporabe
- 4.1 Kot malta
- 4.2 Pri proizvodnji očal
- 4.3 Pri rudarstvu
- 4.4 Kot silikatni odstranjevalec
- 5 Nanodelci kalcijevega oksida
- 6 Reference
Formula
Kemijska formula kalcijevega oksida je CaO, v kateri je kalcij kot kislinski ion (akceptor elektrona) Ca2+, in kisik kot bazni ion (elektronski donor) OR2--.
Zakaj ima kalcij + 2 dajatev? Ker kalcij spada v 2. skupino periodnega sistema (g. Becambara) in ima na voljo le dva valenčna elektrona za tvorbo vezi, ki daje kisikov atom..
Struktura
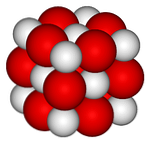
Na zgornji sliki je predstavljena kristalna struktura (tip gem-soli) za kalcijev oksid. Voluminozne rdeče krogle ustrezajo ionom Ca2+ in bele krogle na ione O2-.
V tej kubični razporeditvi kristalov vsak ion Ca2+ je obdana s šestimi ioni O2-, okludirani v oktaedrične luknje, ki jih med njimi puščajo veliki ioni.
Ta struktura izraža maksimalno ionski značaj tega oksida, čeprav izjemna razlika polmerov (rdeča krogla je večja od bele) daje šibkejšo kristalno mrežasto energijo v primerjavi z MgO..
Lastnosti
Fizično je kristalinična bela trdna snov, brez vonja in z močnimi elektrostatičnimi interakcijami, ki so odgovorne za visoka tališča (2572 ° C) in vrelišče (2850 ° C). Poleg tega ima molekulsko maso 55,958 g / mol in zanimivo lastnost, da je termoluminescenčna.
To pomeni, da lahko del kalcijevega oksida, ki je izpostavljen plamenu, zasije z močno belo svetlobo, znano v angleščini z imenom v središču pozornosti, ali v španščini svetloba kalcija. Ioni Ca2+, v stiku z ognjem povzročijo rdečkast plamen, kot je prikazano na naslednji sliki.

Topnost
CaO je bazični oksid, ki ima visoko afiniteto do vode, kolikor absorbira vlago (je higroskopna trdna snov), takoj reagira in proizvaja gašeno apno ali kalcijev hidroksid:
CaO (s) + H2O (l) => Ca (OH)2(s)
Ta reakcija je eksotermna (sprosti toploto) zaradi tvorbe trdne snovi z močnejšimi interakcijami in stabilnejšo kristalno mrežo. Vendar pa je reakcija reverzibilna, če se Ca (OH) segreje2, dehidriranje in osvetljevanje gašenega apna; potem, apno "ponovno rodi".
Nastala raztopina je zelo bazična in če je nasičena s kalcijevim oksidom, doseže pH 12,8.
Prav tako je topen v glicerolu in kislinskih in sladkornih raztopinah. Ker je osnovni oksid, ima naravno učinkovito interakcijo s kislinskimi oksidi (SiO2, Al2O3 in Faith2O3, na primer) je topen v tekoči fazi. Po drugi strani pa je netopen v alkoholih in organskih topilih.
Uporabe
CaO ima veliko število industrijskih uporab kot tudi pri sintezi acetilena (CH≡CH), pri ekstrakciji fosfatov iz odpadne vode in v reakciji z žveplovim dioksidom iz plinastih odpadkov..
Druge uporabe kalcijevega oksida so opisane spodaj: \ t
Kot malta
Če se kalcijev oksid pomeša s peskom (SiO2) in vodo, pecite s peskom in počasi reagirajo z vodo, da nastane gašeno apno. Po drugi strani pa CO2 v vodi raztopi in reagira s soljo, da nastane kalcijev karbonat:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Je bolj odporna in trša spojina kot CaO, zaradi česar malta (prejšnja mešanica) strdi in fiksira opeke, bloke ali keramiko med njimi ali na želeno površino..
V proizvodnji očal
Bistvena surovina za proizvodnjo stekel so silicijevi oksidi, ki se mešajo z apnom, natrijevim karbonatom (Na2CO3) in drugih dodatkov, ki se nato segrejejo, kar povzroči steklasto trdno snov. To trdno snov se nato segreje in piha v vseh številkah.
V rudarstvu
Gašeno apno je zaradi interakcij vodikovih vezi (O-H-O) večje od volumna apna. Ta lastnost se uporablja za lomljenje kamnin od znotraj.
To dosežemo tako, da jih napolnimo s kompaktno mešanico apna in vode, ki je zapečatena, da usmeri svojo toploto in ekspanzivno moč v skalo..
Kot silikatni odstranjevalec
CaO se zliva s silikati, da nastane koalescentna tekočina, ki se nato ekstrahira iz surovine določenega proizvoda..
Na primer, železove rude so surovina za proizvodnjo kovinskega železa in jekla. Ti minerali vsebujejo silikate, ki so nezaželene nečistoče v procesu in se izločajo po opisani metodi.
Nanodelci kalcijevega oksida
Kalcijev oksid se lahko sintetizira kot nanodelci, ki spreminjajo koncentracije kalcijevega nitrata (Ca (NO3)2) in natrijev hidroksid (NaOH) v raztopini.
Ti delci so sferični, osnovni (kakor tudi trdna makro) in imajo veliko površino. Posledično te lastnosti koristijo katalitičnim procesom. Kateri? Preiskave trenutno odgovarjajo na to vprašanje.
Ti nanodelci so bili uporabljeni za sintezo substituiranih organskih spojin, ki izvirajo iz piridinov, pri pripravi novih zdravil za izvajanje kemičnih transformacij, kot je umetna fotosinteza, za čiščenje vode iz težkih in škodljivih kovin ter fotokatalitična sredstva.
Nanodelce lahko sintetiziramo na biološki podpori, kot so listi papaje in zelenega čaja, ki se uporabljajo kot antibakterijsko sredstvo..
Reference
- scifun.org (2018). Apno: kalcijev oksid. Pridobljeno 30. marca 2018, s: scifun.org.
- Wikipedija. (2018). Kalcijev oksid. Pridobljeno 30. marca 2018 od: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Zelena sinteza nanodelcev kalcijevega oksida in njene uporabe. Int. Journal of Engineering Research and Application. ISSN: 2248-9622, zvezek 6, številka 10, (del -1), str.
- J. Safaei-Ghomi et al. (2013). Nanodelci kalcijevega oksida, katalizirani enostopenjska multikomponentna sinteza visoko substituiranih piridinov v vodni etanolni sredini Scientia Iranica, Transakcije C: Kemija in kemijsko inženirstvo.
- PubChem. (2018). Kalcijev oksid. Pridobljeno 30. marca 2018, iz: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Anorganska kemija V Elementi skupine 2. (četrta izdaja, str. 280). Mc Graw Hill.


