Atomski polmer, kako se meri, kako se spreminja v periodnem sistemu, primeri
The atomski polmer je pomemben parameter za periodične lastnosti elementov periodnega sistema. Neposredno je povezana z velikostjo atomov, saj so pri večjem radiju večji ali obsežnejši. Prav tako je povezana z elektronskimi značilnostmi iste.
Dokler ima atom več elektronov, večja je njegova velikost in atomski polmer. Oba sta opredeljena z elektroni valenčne lupine, ker se na razdaljah, ki presegajo njihove orbite, verjetnost iskanja elektrona približuje ničli. Nasprotje se dogaja v bližini jedra: verjetnost iskanja elektrona narašča.

Zgornja slika predstavlja pakiranje bombažnih kroglic. Upoštevajte, da je vsaka obdana s šestimi sosedi, ne da bi štela še eno možno zgornjo ali spodnjo vrstico. Način stiskanja bombažnih kroglic bo določal njihove velikosti in s tem njihove polmere; tako kot se dogaja z atomi.
Elementi po svoji kemijski naravi tako ali drugače delujejo s svojimi atomi. Zato se velikost atomskega polmera spreminja glede na vrsto prisotne vezi in trdno pakiranje njegovih atomov.
Indeks
- 1 Kako merimo atomski polmer?
- 1.1 Določanje medzvočne razdalje
- 1.2 Enote
- 2 Kako se spreminja periodni sistem?
- 2.1 V določenem obdobju
- 2.2 Spuščanje po skupini
- 2.3 Krčenje lantanidov
- 3 Primeri
- 4 Reference
Kako se meri atomski polmer?
Na glavni sliki je lahko enostavno izmeriti premer bombažnih kroglic in ga nato razdeliti za dve. Vendar pa krog atoma ni povsem definiran. Zakaj? Ker elektroni krožijo in razpršujejo v določenih območjih prostora: orbitale.
Zato se atom lahko obravnava kot krogla z neprepustnimi robovi, ki jih ni mogoče z gotovostjo reči, v kolikšni meri se konča. Na primer, v zgornji sliki je središče regije blizu jedra videti bolj intenzivno barvo, robovi pa so zabrisani..
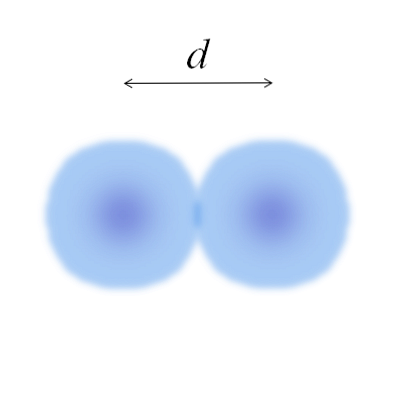
Slika predstavlja diatomno molekulo E2 (kot Cl2, H2, O2, itd.). Ob predpostavki, da so atomi sferični telesi, če je bila razdalja določena d ki loči obe jedri v kovalentni vezi, potem bi bilo dovolj, da jo razdelimo na dve polovici (d/ 2) za pridobitev atomskega polmera; natančneje, kovalentni radij E za E2.
In če E ne oblikuje kovalentnih vezi s samim seboj, ampak je kovinski element? Potem pa d nakazano bi bilo s številom sosedov, ki obkrožajo E v svoji kovinski strukturi; to je s koordinacijsko številko (NC) atoma v embalaži (spomnite se bombažnih kroglic glavne slike).
Določanje medzvočne razdalje
Za določitev d, ki je internuklearna razdalja za dva atoma v molekuli ali embalaži, zahteva fizikalne analize.
Eden od najpogosteje uporabljenih je rentgenska difrakcija, v njej pa se skozi kristal seva svetlobni žarek, preučuje pa se difrakcijski vzorec, ki je posledica interakcij med elektroni in elektromagnetnim sevanjem. Glede na embalažo lahko dobimo različne difrakcijske vzorce in s tem tudi druge vrednosti d.
Če so atomi v kristalni rešetki "tesni", bodo predstavili različne vrednosti d v primerjavi s tem, kar bi imeli, če bi bili "udobni". Tudi te med-jedrne razdalje lahko nihajo v vrednostih, tako da atomski polmer dejansko sestoji iz povprečne vrednosti takih meritev..
Kako so povezani atomski polmer in koordinacijsko število? V. Goldschmidt je vzpostavil razmerje med obema, pri čemer je za N. 12 relativna vrednost 1; od 0,97 za pakiranje, kjer ima atom N.C enak 8; 0,96, za NC enako 6; in 0,88 za NC 4.
Enote
Iz vrednosti za N.C, ki je enaka 12, je bilo izdelanih veliko tabel s primerjavo atomskih polmerov vseh elementov periodne tabele..
Ker vsi elementi ne tvorijo takšnih kompaktnih struktur (N. manj kot 12), se razmerje V. Goldschmidt uporablja za izračunavanje njihovih atomskih polmerov in njihovo izražanje za isto pakiranje. Na ta način so meritve atomskih radijev standardizirane.
Toda v katerih enotah se izražajo? Od takrat d je zelo majhna, je treba uporabiti enote angstroma Å (10. 10)-10m) ali pa se pogosto uporablja, pikometer (10. 10)-12m).
Kako se spreminja v periodnem sistemu?
V celotnem obdobju
Atomski polmeri, določeni za kovinske elemente, dobijo ime kovinskih polmerov, medtem ko so za tiste nekovinske elemente kovalentni polmeri (kot je fosfor, P)4, ali žveplo, S8). Vendar pa je med obema vrstama radijskih postaj vidnejše razlikovanje kot ime.
Od leve proti desni v istem obdobju jedro dodaja protone in elektrone, vendar so slednji omejeni na enako raven energije (glavno kvantno število). Posledica tega je, da jedro narašča efektivni jedrski naboj na valentnih elektronih, ki se vežejo na atomski polmer.
Na ta način imajo ne-kovinski elementi v istem obdobju običajno manjše atomske (kovalentne) polmere kot kovine (kovinski polmeri)..
Spuščanje skupine
Ko se spuščamo s skupino, omogočimo nove ravni energije, ki omogočajo, da imajo elektroni več prostora. Tako elektronski oblak prekriva večje razdalje, njegova zamegljena periferija se bolj oddaljuje od jedra in se zato atomski polmer širi..
Krčenje lantanidov
Elektroni notranje plasti pomagajo zaščititi učinkovit jedrni naboj na valentnih elektronih. Ko imajo orbitale, ki sestavljajo notranje plasti, veliko "lukenj" (vozlišč), kot pri f orbitaleh, jedro močno skrči atomski polmer zaradi slabega zaščitnega učinka orbitalov..
To dejstvo je dokazano v krčenju lantanida v obdobju 6 periodnega sistema. Iz La v Hf obstaja precejšnje krčenje atomskega polmera, ki ga proizvajajo orbitale f, ki se "napolnijo", ko gre skozi blok f: tisto za lantanoide in aktinoide.
Podoben učinek lahko opazimo tudi pri elementih bloka p iz obdobja 4. Ta časovni produkt šibkega zaščitnega učinka orbitalov d, ki se napolnijo pri prehodu med prehodnimi kovinami.
Primeri
Za obdobje 2 periodne tabele so atomski polmeri njegovih elementov:
-Li: 257 ur
-Bodite: 112 ur
-B: 88 pm
-C: 77 pm
-N: 74 pm
-O: 66 ur
-F: 64 p.m.
Upoštevajte, da ima litijeva kovina največji atomski radij (257 p.m), medtem ko je fluor, ki se nahaja na skrajni desni strani obdobja, najmanjši od njih (64 ppm). Atomski polmer se v istem obdobju spušča od leve proti desni in prikazane vrednosti kažejo.
Litij, s tvorbo kovinskih vezi, je njegov polmer kovinski; in fluor, ker tvori kovalentne vezi (F-F), njegov polmer je kovalenten.
In če želite izraziti atomske radijske postaje v enotah angstroma? Preprosto jih razdelimo s 100: (257/100) = 2.57Å. In tako naprej s preostalimi vrednotami.
Reference
- Kemija 301. Atomska radija. Vzpostavljeno iz: ch301.cm.utexas.edu
- Fundacija CK-12. (28. junij 2016). Atomski polmer. Vzpostavljeno iz: chem.libretexts.org
- Trendi v atomskem radiju. Vzeto iz: intro.chem.okstate.edu
- Clackamas Community College. (2002). Atomska velikost. Vzpostavljeno iz: dl.clackamas.edu
- Clark J. (avgust 2012). Atomski in ionski polmer. Vzpostavljeno iz: chemguide.co.uk
- Shiver & Atkins. (2008). Anorganska kemija (Četrta izdaja., Str. 23, 24, 80, 169). Mc Graw Hill.


