Joseph Thomson Biografija in prispevki k znanosti in kemiji
Joseph John Thomson Bil je pomemben kemik za različne prispevke, kot so odkritje elektrona, njegov atomski model, odkritje izotopov ali katodni preskus..
Rodil se je 18. decembra 1856 v Cheetam Hillu v okrožju Manchester v Angliji. Znan je bil tudi kot J.J. Thomson..

Leta 1890 se je J. J. Thomson poročil z Rose Elizabeth Paget, hčerko zdravnika Sir Edwarda Georgea Pageta, s katero sem imel dva otroka: deklico Joan Paget Thomson in fanta, Georgea Pageta Thomsona..
Slednji bi postal znan znanstvenik, ki je dobil leta 1937 Nobelovo nagrado za fiziko za svoje delo z elektroni.
Thomson je že v mladosti svoje študije osredotočil na strukturo atomov in tako odkril obstoj elektronov in izotopov, med mnogimi drugimi prispevki..
Leta 1906 je Thomson prejel Nobelovo nagrado za fiziko, "za priznanje velike zasluge svojih teoretičnih in eksperimentalnih raziskav o prevajanju električne energije skozi pline", med številnimi drugimi nagradami za svoje delo. (1)
Leta 1908 ga je britanska krona razglasila za vitez in bila častna profesorica fizike na Cambridgeu in na Kraljevem inštitutu v Londonu.
Umrl je 30. avgusta 1940, leta 83, v mestu Cambridge, Velika Britanija. Fizik je bil pokopan v opatiji Westminster, blizu groba Sir Isaaca Newtona. (2)
Indeks
- 1 Glavni prispevki Thomsona k znanosti
- 1.1 Odkritje elektrona
- 1.2 Thomsonov atomski model
- 1.3 Ločevanje atomov
- 1.4 Odkrivanje izotopov
- 1.5 Poskusi s katodnimi žarki
- 1.6 Masni spektrometer
- 2 Zapuščina podjetja Thomson
- 3 Izbrana dela
- 4 Reference
Glavni prispevki Thomsona k znanosti
Odkritje elektrona
Leta 1897 je J.J. Thomson je odkril nov delček, lažji od vodika, ki je bil krstil "elektron".
Vodik je veljal za enoto merjenja atomske teže. Do takrat je bil atom najmanjša delitev snovi.
V tem smislu je bil Thomson prvi odkril negativno nabite corpuscular subatomske delce.
Atomski model Thomsona
Thomsonov atomski model je bila struktura, ki jo je angleški fizik pripisal atomom. Za znanstvenika so atomi sfera pozitivnega naboja.
Tam so bili negativno nabiti elektroni, enakomerno porazdeljeni po tem pozitivno obremenjenem oblaku, vgrajeni in nevtralizirali pozitivni naboj mase atoma..
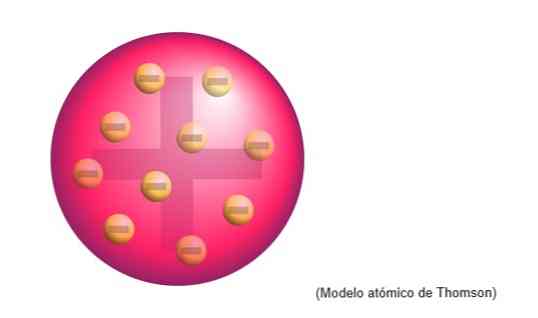
Ta novi model nadomešča model, ki ga je izdelal Dalton, kasneje pa ga bo zavrnil Rutherford, učenec Thomsona v laboratorijih Cavendish iz Cambridgea..
Ločevanje atomov
Thomson je uporabil pozitivne ali anodne žarke za ločevanje atomov različne mase. Ta metoda mu je omogočila izračun električne energije, ki jo prenaša vsak atom, in število molekul na kubični centimeter.
Fizik je z zmožnostjo delitve atomov različne mase in naboja odkril obstoj izotopov. Tudi na ta način je s študijo pozitivnih žarkov naredil velik napredek v smeri masne spektrometrije.
Odkritje izotopov
J.J. Thomson je odkril, da imajo neoni ioni različne mase, torej različne atomske uteži. Tako je Thomson pokazal, da neon ima dva podtipa izotopov, neon-20 in neon-22..
Izotopi, ki so do danes proučeni, so atomi istega elementa, vendar imajo njihova jedra različna masna števila, saj so sestavljena iz različnih količin nevtronov v svojem središču..
Poskusi s katodnimi žarki
Katodni žarki so elektronski tokovi v vakuumskih ceveh, to je steklene cevi z dvema elektrodama, eno pozitivno in eno negativno.
Če se negativna elektroda, ali imenovana tudi katoda, segreje, oddaja sevanje, ki je usmerjeno proti pozitivni elektrodi ali anodi, v ravni liniji, če na tej poti ni magnetnega polja..
Če so stene cevnega stekla prekrite s fluorescentnim materialom, se pri udarcu katode proti tej plasti postavi projekcija svetlobe.
Thomson je preučil obnašanje katodnih žarkov in prišel do zaključkov, da se žarki širijo v ravni črti.
Tudi, da bi se ti žarki lahko odstopili od njihove poti s prisotnostjo magneta, to je magnetnega polja. Poleg tega lahko žarki premikajo žile s silo mase elektronov, ki krožijo, kar dokazuje, da imajo elektroni maso.
J.J. Thomson je poskusil spreminjati plin znotraj katodne cevi, vendar se obnašanje elektronov ni razlikovalo. Prav tako so katodni žarki segreli predmete, ki so stali med elektrodami.
Na koncu je Thomson pokazal, da imajo katodni žarki svetlobne, mehanske, kemijske in toplotne učinke.
Katodne cevi in njihove svetlobne lastnosti so bile transcendentne za kasnejši izum cevne televizije (CTR) in video kamer..
Masni spektrometer
J.J. Thomson je ustvaril prvi pristop masni spektrometer. To orodje je znanstveniku omogočilo, da preuči razmerje masa / naboj katodnih cevi in izmeri, koliko jih preusmeri vpliv magnetnega polja in količino energije, ki jo prenašajo..
S temi raziskavami je prišel do zaključka, da so katodni žarki sestavljeni iz negativno nabitih krvnih celic, ki so znotraj atomov, s čimer se postulira delljivost atoma in povzroči nastanek številke elektrona..
Prav tako se je napredek v masni spektrometriji do danes nadaljeval in se razvijal v različnih metodah za ločevanje elektronov od atomov.
Poleg tega je Thomson prvi predlagal prvi valovod leta 1893. Ta poskus je obsegal razmnoževanje elektromagnetnih valov v nadzorovani valjasti votlini, ki jo je leta 1897 prvič izvedel Lord Rayleigh, druga Nobelova nagrada za fiziko..
Valovodi bi se v prihodnosti pogosto uporabljali, tudi danes s prenosom podatkov in optičnimi vlakni.
Zapuščina Thomsona
Thomson (Th) je bil ustanovljen kot enota za merjenje masne obremenitve v masni spektrometriji, ki so jo predlagali kemiki Cooks in Rockwood v čast Thomsonu.
Ta tehnika omogoča določanje porazdelitve molekul snovi glede na njegovo maso in, ki jo prepozna, ki so prisotne v vzorcu snovi..
Thomsonova formula (Th):

Izbrana dela
- Razprodaja električne energije skozi pline, vodenje električnih plinov (1900).
- Telesna teorija materije, Elektron v kemiji in spominih in refleksijah (1907).
- Beyond the Electron (1928).
Reference
- Nobel Media AB (2014). J. Thomson - Biografski. Nobelprize.org. nobelprize.org.
- Thomson, Joseph J., Vodenje električne energije prek plinov. Cambridge, University Press, 1903.
- Menchaca Rocha, Arturo. Diskreten čar elementarnih delcev.
- Christen, Hans Rudolf, Osnove splošne in anorganske kemije, Zvezek 1. Barcelona, Španija. Ediciones Reverté S.A., 1986.
- Arzani, Aurora Cortina, Splošna elementarna kemija. Mehika, uredništvo Porrúa, 1967.
- R. G. Cooks, A. L. Rockwood. Rapid Commun. Masni spekter. 5, 93 (1991).


